Кафедра генетики спбгу адрес
В 1932г. по инициативе Н.И.Вавилова на биологическом факультете была открыта кафедра генетики растений, которой заведовал Г.Д.Карпетченко (1899-1942), курс цитологии на этой кафедре читал проф. Г.А.Левитский – первый цитолог России, курс основ селекции растений читал Л.И.Говоров, курс экспериментальных основ систематики растений – М.А.Розанова. Кафедра генетики растений фактически прекратила активную работу после ареста в 1940г. Н.И.Вавилова, а в 1941г. Г.Д.Карпетченко, Г.А.Левитского, Л.И.Говорова. Все они погибли, но впоследствии были посмертно реабилитированы. В 1941г. многие молодые сотрудники, аспиранты и студенты обеих кафедр ушли добровольцами на фронт. Через три года после окончания войны, в 1948г., прошла августовская сессия Всесоюзной Академии Сельскохозяйственных Наук им. В.И.Ленина, завершившая разгром отечественной генетики и биологии в целом. В числе уволенных из Университета оказались генетик М.Е.Лобашев (в то время декан биологического факультета), бывший заведующий кафедрой генетики (1938-1940) проф. Ю.И.Полянский (в то время и.о.ректора университета) и эмбриолог П.Г.Светлов, заведующий кафедрой генетики (1944-1948). Заведующим объединенной кафедрой генетики и селекции (1948-1954) стал проф. Н.В.Турбин. Официальный запрет на преподавание генетики и публикацию экспериментальных работ менделистами-вейсманистами просуществовал около 10 лет.
В 1957г. заведующим кафедрой генетики и селекции Ленинградского университета был избран по конкурсу проф. М.Е.Лобашев (1907-1971), который после долгого перерыва начал читать нормальный курс генетики с основами селекции для студентов биолого-почвенного факультета, объединивший классическую, биохимическую и молекулярную генетику. Уже тогда на кафедре были две специализации: генетика растений и генетика животных, а в 1959г. организована специализация генетика микроорганизмов, заложившая основы исследований по молекулярной генетике. С 1961г. М.Е.Лобашев издает сборник «Исследования по генетике», в котором публикуются экспериментальные работы кафедры и теоретические обзорные статьи. В 1963г. выходит первый современный отечественный учебник М.Е.Лобашева «Генетика». С 1972 г кафедрой генетики и селекции заведует профессор, академик РАН С.Г.Инге-Вечтомов.
Кафедра генетики спбгу адрес
Выпускники кафедры успешно работают в научных учреждениях и биотехнологических фирмах России, США, Германии, Франции и других стран мира.
Сотрудники, студенты и аспиранты кафедры принимают участие в различных международных и российских конференциях. В настоящее время на кафедре выполняется более 20 грантов, восемь из которых являются индивидуальными грантами для молодых ученых.
Сегодня на кафедре генетики учится более 50 студентов и аспирантов. Многие из них выполняют экспериментальную работу на кафедре, начиная с первого курса, и к моменту поступления в магистратуру или аспирантуру являются авторами одной или нескольких публикаций.
Кафедра работает в тесном сотрудничестве с Санкт-Петербургским Филиалом Института общей генетики им. Н.И.Вавилова РАН ( СПбФ ИОГен РАН ), организованным в 2005г. на базе кафедры генетики и селекции СПбГУ.
В 2003 г. сотрудниками кафедры был основан журнал “ Экологическая генетика ”.
Научная работа на кафедре организована по трем специализациям: генетика микроорганизмов, генетика растений, генетика животных, кроме того, многие студенты выполняют квалификационные работы в различных академических и медицинских институтах. Наряду с традиционными генетическими методами студенты кафедры активно овладевают различными современными методами флуоресцентной микроскопии, молекулярной генетики, генной инженерии, компьютерной обработки данных, филогенетики. Лаборатории оснащены современным оборудованием, которое активно используется студентами и постоянно обновляется. Кафедра активно сотрудничает с научными учреждениями Санкт-Петербурга (Институт цитологии РАН, Зоологический институт РАН, институт сельскохозяйственной микробиологии, институт акушерства и гинекологии и др.), и Москвы (Институт биохимии им.А.Н.Баха РАН, институт молекулярной биологии РАН). Проводятся совместные исследования с научными лабораториями США, Франции, Германии, Нидерландов, Великобритании, в которых активно участвуют студенты и аспиранты кафедры.
Кафедра генетики спбгу адрес
Кафедра участвует в чтении следующих общефакультетских курсов:
• Введение в биологию
• Общая генетика
• Общая и экологическая генетика
• Молекулярная биология
• Биотехнология и генная инженерия
• Симбиоз и симбиогенез
• Геномика и геносистематика
Бакалавриат.
Начальная специализация в бакалавриате кафедры осуществляется по направлениям «Генетика микроорганизмов», «Генетика животных», «Генетика растений».
Курсы и практикумы начальной специализации бакалавриата
• Генетический анализ
• Генетика прокариот
• Математические методы в генетике
• Генетика человека
• Цитогенетика
• Генетика эукариот
• Генетика органелл
• Генетика популяций и охрана генофонда
• Практикум по методам генетического анализа
• Практикум по основным генетическим методам
Летние учебные практики:
• Практикум по генной инженерии
Магистратура.
Дальнейшая специализация проходит в магистратуре по профилю «Генетика, молекулярная генетика».
Основные курсы магистратуры:
• Медицинская генетика
• Мутационный процесс
• Экологическая генетика
• Генетика развития растений
• Генетика развития животных
• Генетический контроль клеточного цикла
• Транскрипция и мир РНК
• Онкогенетика и пути сигнальной трансдукции
• Метагеномика
• Эволюция человека
• Цитогенетика и генетика эмбрионального развития человека
• Молекулярно-генетические механизмы адаптации растений
• Мобильные элементы генома
• Апоптоз
• Актуальные проблемы молекулярной биотехнологии растений
• Генетический контроль трансляции
• Посттрансляционная судьба белков
• Протеомика
• Молекулярные основы эволюции
• Ретроспективы генетики
• Практикум по генной и клеточной инженерии растений
• Молекулярно-биохимические методы (практикум)
• Цитогенетические методы тестирования действия факторов окружающей среды
Программа вступительных экзаменов в аспирантуру
Кафедра генетики спбгу адрес
Лаборатория генной и клеточной инженерии растений организована в 2000 г. Исследования охватывают широкий спектр объектов, опираются как на современные методы молекулярной биологии (включая молекулярное маркирование, ПЦР в реальном времени, секвенирование, инсерционный мутагенез), так и на традиционные — методы генетического анализа, тестирование физиологических признаков in vitro и другие.
Генетический контроль развития меристем
Известно, что основную роль в развитиии меристем играют несколько групп регуляторных генов:
1. меристем-специфичных генов семейств KNOX и WOX, кодирующих гомеодомен-содержащие транскрипционные факторы;
2. гены, кодирующие компоненты систем CLAVATA, регулирующих экспрессию генов WOX;
3. гены, регулирущие метаболизм фитогормонов, главным образом – цитокининов и ауксинов.
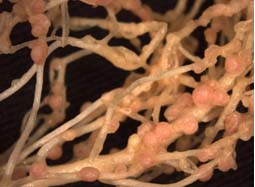
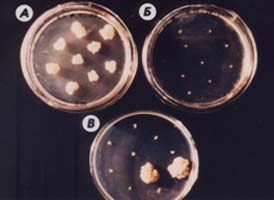
Рис.1 Корнеплоды редиса с опухолями.
Рис.2 Корни с клубеньками суперклубенькообразующего мутанта гороха.
Мы идентифицировали гены, кодирующие меристемные регуляторы разных групп, проведено сравнительное изучение их экспрессии при развитии меристем разных типов и локальный анализ их экспрессии в меристемах (Рис. 3). Это позволило определить гены-кандидаты на роль универсальных регуляторов развития меристем. Эксперименты по сверхэкспрессии и сайленсингу выявленных генов-кандидатов подтвердили наши предположения об универсальности некоторых механизмов регуляции групп стволовых клеток в разных типах меристем, а также составить предполагаемые схемы взаимодействия разных факторов (например – фитогормонов и транскрипционных факторов) в их регуляции.
Одним из таких универсальных меристемных регуляторов является ген WOX5, кодирующий гомеодомен-содрежащий транскрипционный фактор. Ранее была выяснена его функция как регулятора пула стволовых клеток в меристеме корня. В наших исследованиях была показана роль WOX5 как центрального регулятора меристемы клубенька и мишени системы авторегуляции клубенькообразования. Также была отмечена роль этого гена в развитии спонтанных опухолей у линий редиса и опухолей, индуцированных агробактериями. Таким образом, в наших исследованиях был выявлен универсальный регулятор развития меристем корня – ген WOX5.
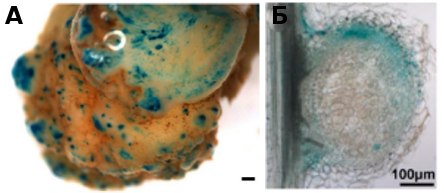
Рисунок 3. Локальный анализ экспрессии гена WOX5 в спонтанных опухолях редиса(A) и в симбиотических клубеньках гороха (Б).
Центральную роль в регуляции экспрессии генов WOX играют системы CLAVATA, включающие в себя семейство регуляторных пептидов CLE, их рецепторы и нижележащие компоненты сигналинга. Нами впервые идентифицирована роль некоторых CLE-пептидов в развитии опухолей у растений и вторичном росте корня, а также исследовано их взаимодействие с фитогормонами цитокининами.
Генетический контроль соматического эмбриогенеза у растений
Соматический эмбриогенез – это вид регенерации растений, при котором наблюдается образование эмбрионов из соматических клеток, без оплодотворения. Соматические эмбрионы у большинства видов развиваются in vitro на поверхности эмбриогенного каллуса – скопления недифференцированных клеток. Цель работы – выявить механизм, определяющий те конкретные клетки каллуса, которые дадут начало соматическим эмбрионам (Рис. 4).

Рисунок 4. Соматический эмбрион люцерны.
Объектом исследования являются генетические линии люцерны (Medicago truncatula) с повышенной способностью к соматическому эмбриогенезу in vitro. Мы исследуем работу транскрипционных факторов из семейства WOX, а также транспортёров ауксина из семейства PIN в соматическом эмбриогенезе. Некоторые из генов WOX и PIN участвуют в регуляции ранних этапов обычного зиготического эмбриогенеза — развития зародыша после оплодотворения.
К настоящему времени нами показано, что в ходе соматического эмбриогенеза повышается уровень экспрессии тех же генов WOX, которые активируются при развитии зиготического эмбриона. Ведётся работа по получению трансгенных растений M.truncatula для визуализации экспрессии интересующих нас генов WOX и PIN.
Получение растений, устойчивых к болезням и вредителям сельского хозяйства
Известно, что насекомые-вредители, некоторые патогены (например, возбудитель фитофтороза) и другие неспособны к самостоятельному синтезу стеринов, а потому целиком зависят от их содержания в пище. Недостаток стеринов в пище резко отражается на развитии и репродуктивной способности этих объектов.
Рис.5. Результаты селекции каллусов табака на среде с полиеновыми антибиотиками.
Рис.6. Регенерация побегов картофеля после агротрансформации.
Наша работа, начатая совместно с лабораторией генетики животных, посвящена получению растений, обладающих устойчивостью к вредителям сельского хозяйства. Для достижения поставленной цели мы используем методы опосредованной клеточной селекции (Рис.5,6), и методы генной инженерии с целью получения растений с измененным метаболизмом фитостеринов, необходимых для развития насекомых-вредителей.
Изучение горизонтального переноса генов от агробактерий к растениям
Известно, что некоторые растения содержат в своих геномах последовательности, гомологичные Т-ДНК из агробактерий, наиболее распространенного вектора для перенесения чужеродной ДНК в растения.
Некоторые гены Ri-плазмиды Agrobacterium rhizogenes (rol гены) присутствуют в ряде видов рода Nicotiana (Рис. 7) как результат горизонтального переноса генов в эволюции данного рода растений.
Рис.7. Примеры видов табака, в геноме которых присутствуют гены агробактерии: rolC, rolB, ORF13, ORF14
В нашей лаборатории впервые в результате целенаправленного поиска Т-ДНК-подобных последовательностей у представителей двудольных растений обнаружен новый пример горизонтального переноса генов от агробактерий к растениям рода Linaria. Т-ДНК-подобные последовательности L. vulgaris детально охарактеризованы и обнаружены некоторые общие закономерности в структуре Т-ДНК у табаков и льнянок.
Описание гомологов агробактериальных генов в дикорастущих видах позволит снизить обеспокоенность экологов и населения относительно возможного негативного влияния «трансгенизации» на здоровье людей и окружающей среды.
Создание растений-продуцентов γ-интерферона быка
γ-интерферон, который широко применяют в медицине и ветеринарии – естественный иммуномодулятор, участвующий в формировании естественного и специфического иммунитета.
В настоящее время препарат бычьего гамма-интерферона используют для профилактики туберкулёза и лейкемии крупного рогатого скота. Создание растений-продуцентов гамма-интерферона быка позволит избежать ежегодного трудоёмкого процесса вакцинации молодых бычков, используя данные растения-продуценты в качестве «вакцин».
В совместной работе с лабораторией биохимической генетики лаборатории, с помощью агробактериальной транформации получены растения табака (Nicotiana tabacum L.), содержащие ген бычьего γ-интерферона. Проводятся работы по получению сельскохозяйственных растений (гороха и моркови), синтезирующих данный белок. Эти растения могут быть использованы как иммуностимулирующая пищевая добавка к рациону крупного рогатого скота.
Генетика метаболизма хлорофиллов
Хлорофиллы – уникальные природные тетрапирролы, играющие ключевую роль не только в жизни фотосинтезирующих организмов, но и всей биосферы. Их биосинтез связан с морфогенезом растительной клетки и реакциями фотосинтеза – запасанием и передачей энергии света.
Важнейшая фундаментальная проблема современной биологии состоит в понимании природы процесса биосинтеза хлорофилла, механизмов его генетической и биохимической регуляции, а также закономерностей изменений, которые они претерпели в ходе эволюции и при адаптации к различным условиям.
Экспериментальные исследования ведутся на пигментных мутантах зелёной одноклеточной водоросли Chlamydomonas reinhardtii (Chlamy)– модельного объекта генетики фотосинтеза (Рис. 8). Её клетки, в отличие от высших растений, синтезируют хлорофилл не только на свету, но и в гетеротрофных условиях (в темноте), используя в качестве источника углерода ацетат натрия. Такая способность позволяет получать мутанты по обоим путям биосинтеза: темновому и индуцируемому светом.
Рис 8. Клетки Chlamydomonas reinhardtii
Штаммы из коллекции активно используются в экспериментальных исследованиях, педагогическом процессе (Летняя практика по генетике и в курсе “Генетика микроводорослей”), создании штаммов-продуцентов биологически-активных веществ и разработке тест-систем оценки экологической безопасности водных ресурсов.
Основные результаты исследований
Осуществлена молекулярно-генетическая идентификация генов, контролирующих ключевой фермент в цепи биосинтеза хлорофилла — магний-хелатазу. Структурный ген CHLH хламидомонады, кодирует большую (H) субъединицу магний-хелатазы. Исследованы его структура и функции.
Обнаружен новый регуляторный ген LTS3 C. reinhardtii, кодирующий фактор транскрипции семейства GATA – активатор транскрипции генов Mg-хелатазы в темноте. Молекулярно-генетические исследования мутантов по гену LTS3 позволили установить, что белок Chlamy LTS3 – первый, обнаруженный у водорослей фактор транскрипции семейства GATA, непосредственно регулирующий экспрессию генов биосинтеза хлорофилла. Сам факт его существования свидетельствует, что темновой БХ может обеспечиваться регуляторными элементами, действующими на уровне транскрипции.
Изучение супрессии мутаций в гене LTS3 привело к обнаружению еще одного ранее неизвестного гена – SUP-I, продукт которого является ядерным регуляторным белком-активатором экспрессии гена LTS3 и необходим для процесса зеленения – индуцированного светом синтеза хлорофилла.
Описан новый хлоропластный ген хламидомонады mod-u-25, участвующий в процессе регуляции уровня содержания ПП в клетке.
• Лаборатория биохимической генетики СПбГУ
• Институт цитологии и генетики, Новосибирск
Виноградова А.П., Лебедева (Осипова) М.А., Лутова Л.А. Меристематические характеристики опухолей, индуцированных Agrobacterium tumefaciens у гороха. Генетика. 2015. Т. 51. № 1. C. 1-9.
Лутова Л.А., Додуева И.Е., Лебедева М.А., Творогова В.Е. Транскрипционные факторы в генетике развития и эволюции высших растений. Генетика. 2015. Т. 51. № 3.
Додуева И.Е., Ганчева М.С., Осипова М.А., Творогова В.Е., Лутова Л.А. Латеральные меристемы высших растений: фитогормональный и генетический контроль. Физиология растений. 2014. Т. 61. № 5. С. 1-21.
Lebedeva (Osipova) M.A., Tvorogova V.E., Vinogradova A.P., Gancheva M.A., Azarakhsh M., Ilina E.L. et al. Initiation of spontaneous tumors in radish (Raphanus sativus): Cellular, molecular and physiological events. Journal of Plant Physiology. 2014. V. 173. P. 97-104.
Додуева И.Е., Кирюшкин А.С., Осипова М.А., Юрлова Е.В., Бузовкина И.С., Лутова Л.А. Влияние цитокининов на экспрессию генов CLE редиса. Физиология растений. 2013. т. 60. №2. с. 1-9
Додуева И.Е., Юрлова Е.В., Осипова М.А., Лутова Л.А. CLE-пептиды – универсальные регуляторы развития меристем. Физиология растений. 2012. т. 59. с. 17-31.
Творогова В.Е., Осипова М.А., Додуева И.Е., Лутова Л.А. Взаимодействие транскрипционных факторов и фитогормонов в регуляции активности меристем растений. Экологическая генетика. 2012. №. 3. С. 28-40
Osipova M.A., Mortier V., Demchenko K.N., Tsyganov V.E., Tikhonovich I.A., Lutova L.A. et al. WUSCHEL-RELATED HOMEOBOX5 gene expression and interaction of CLE peptides with components of the systemic control add two pieces to the puzzle of autoregulation of nodulation. Plant Physiology. 2012. V. 158. P. 1329-1341.
Осипова М.А., Долгих Е.А., Лутова Л.А. Особенности экспрессии меристем-специфичного гена WOX5 при органогенезе клубеньков бобовых растений. Онтогенез. 2011. т. 42. с. 1-13.
Dolgikh E.A., Leppyanen I.V., Osipova M.A., Savelyeva N.V., Borisov A.Y., Tsyganov V.E. et al. Genetic dissection of Rhizobium-induced infection and nodule organogenesis in pea based on ENOD12A and ENOD5 expression analysis. Plant Biology. 2011. V. 13 (2). P. 285–296.
Генетический контроль соматического эмбриогенеза у растений
Творогова В.Е., Лебедева М.А., Лутова Л.А. Выявление генов WOX и PIN, участвующих в соматическом эмбриогенезе у Medicago truncatula. Генетика. 2015. В печати.
Изучение горизонтального переноса генов от агробактерий к растениям
Matveeva T.V., Lutova L.A. Horizontal gene transfer from Agrobacterium to plants. Frontiers in Plant Science. 2014. V. 5.
Кулаева О.А., Матвеева Т.В., Лутова Л.А. Изучение возможного горизонтального переноса генов от агробактерий к некоторым представителям семейства Solanaceae. Экологическая генетика. 2013. Т. 11. № 2. С. 3-9.
Павлова О.А., Матвеева Т.В., Лутова Л.А. Геном Linaria dalmatica содержит гомолог гена rolC Agrobacterium rhizogenes. Экологическая генетика. 2013. Т. 11. № 2. С. 10-15.
Matveeva T.V., Bogomaz D.I., Pavlova O.A., Nester E.W., Lutova L.A. Horizontal gene transfer from genus Agrobacterium to the plant Linaria in nature. Molecular Plant-Microbe Interactions. 2012. V. 25. N. 12. P. 1542-155.
Матвеева Т.В., Павлова О.А., Богомаз Д.И., Демкович А.Е., Лутова Л.А. Молекулярные маркеры для видоидентификации и филогенетики растений. Экологическая генетика. 2011. Т. 9. № 1. С. 32-43.
Burlakovskiy M.S., Saveleva N.V., Yemelyanov V.V., Padkina M.V., Lutova L.A. Production of bovine interferon-γ in transgenic tobacco plants. Plant Cell. Tissue and Organ Culture (PCTOC): Journal of Plant Biotechnology. 2015. In Press.
Ткаченко А.А., Емельянов В.В., Савельева Н.В., Лутова Л.А. Конструирование векторов для экспрессии гетерологичного гена гамма-интерферона в растениях гороха посевного (Pisum sativum L.). Биомика. 2012. Т. 3, № 1. С. 103-105.
Савельева Н.В., Лутова Л.А. Растения — продуценты рекомбинантных белков медицинского назначения. Продуценты γ-интерферона быка. Изд. LAPLAMBERT Academic Publishing. 2010. 152с.
Чекунова Е.М. Генетика метаболизма хлорофиллов. LAP LAMBERT Academic Publishing. 2011. 136 с.
Чекунова Е.М., Савельева Н.В. Ген LTS3 контролирует светонезависимый биосинтез хлорофилла у зеленой водоросли Chlamydomonas reinhardtii. Экологическая Генетика. 2010. №2. С.35-44.
Чекунова Е.М. Генетика биосинтеза хлорофилла: Темновой и светонезависимый пути. Экологическая генетика. 2010. №3. С. 38-51.
Кафедра генетики спбгу адрес
Куратор коллекции: Ольга Вадимовна Иовлева
(тел. (812)428-40-08, e-mail: )
Лаборатория генетики животных поддерживает коллекцию, включающую около 100 линий Drosophila melanogaster, в которую входят стандартные линии дикого типа, линии, маркированные по хромосомам Х, 2 и 3, множественно маркированные линии, балансерные линии и линии, несущие хромосомные аберрации. Эта коллекция активно используется в экспериментальной работе, а также при проведении практических занятий студентов.
В коллекцию также входит набор родственных инбредных (более 960-ти поколений инбредного разведения) линий D. melanogaster, полученных Л.З. Кайдановым с сотрудниками путем селекции на различия по репродуктивной функции (Кайданов и др., 1997). Эта работа началась в середине 60х годов прошлого века, селекция линий сопровождалась тесным инбридингом. В результате были отобраны особи, давшие начало линии НА, харакетеризующейся низкой половой активностью самцов, а также целым комплексом генетически контролируемых изменений, важнейшие из которых затронули нейроэндокринную систему дрозофил. Эта линия НА являтся своего рода «родоначальницей» всей коллекции. Линии ВА и НА+ (высокоактивные) получены путем возвратного отбора на повышение половой активности самцов из линии НА на 70-м и 263-м поколениях инбредного разведения линии НА соответственно.
В результате длительной селекции линий НА и ВА на различия по репродуктивной функции в низкоадаптивной линии НА произошло формирование комплекса генетически контролируемых изменений. Для линии НА были показаны: низкая активность ювенильного гормона и изменение его метаболизма, низкое содержание универсального клеточного регулятора цАМФ, ненормальный спектр ацетилхолинэстеразы, низкая общая активность эстеразы-6, измененный состав нейропептидов мозга, высокий уровень перекисного окисления липидов, низкая активность щелочной фосфатазы, которая контролирует содержание биогенных аминов (дофамина и октопамина) у дрозофилы. Низкоактивные линии отягощены грузом летальных, полулетальных и субвитальных мутаций, а также демонстрируют своеобразное распределение мобильных элементов по геному.
Использование уникальной коллекции родственных высокоинбредных линий D. melanogaster позволяет изучать генетические последствия отбора и инбридинга, источники генетической гетерогенности в условиях жесткого инбридинга, темпы мутирования в линиях, различающихся по адаптивной ценности, закономерности перемещений мобильных генетических элементов и их участие в формировании компенсационного комплекса генов, противодействующего последствиям отбора в минус-направлении.
Куратор коллекции: Сергей Павлович Задорский (тел. (812)428-65-70, e-mail: )
Ссылки на описание коллекции:
Андрианова В.М., Инге-Вечтомов С.Г. Каталог (указатель) Петергофской генетической коллекции дрожжей Saccharomyces cerevisiae. Ленинград, 1988.
Самсонова М.Г., Андрианова В.М., Борщевская, Т.Н., Чунаев, А.С. Петергофские генетические коллекции микроорганизмов. Генетика. 1994. 30(8). с. 1123-1129.
Andrianova V.M., Samsonova M.G., Sopova Y.V., Inge-Vechtomov S.G. Catalogue of Peterhof genetic collection of yeast Saccharomyces cerevisiae. St Petersburg, 2003.
Drozdova P.B., Tarasov O.V., Matveenko A.G., Radchenko E.A., Sopova J.V., Polev D.E., Inge-Vechtomov S.G., Dobrynin P.V. Genome Sequencing and Comparative Analysis of Saccharomyces cerevisiae Strains of the Peterhof Genetic Collection. PLoS One. 2016. 11(5). p.e0154722.
Петергофская генетическая коллекция штаммов дрожжей (ПГК) основана в 1972 г. в лаборатории физиологической генетики. В настоящее время ПГК содержит более 300 штаммов пекарских дрожжей Saccharomyces cerevisiae, маркированных различными мутациями и применяемых в генетических экспериментах различной направленности. Особый интерес представляет набор штаммов для быстрого определения хромосомы, в которой произошла наследуемая мутация, а также для картирования мутаций по отношению к центромерам и маркерам некоторых групп сцепления (хромосомы III,IV,VII,VIII). Кроме этого в коллекции представлены штаммы с мутациями, маркирующими аппарат терминации трансляции, тестерные штаммы для исследования мутагенеза, мутанты по клеточному циклу (cdc), а также доноры и реципиенты для цитодукции и α-теста, используемого в генетической токсикологии. Наконец, в коллекции представлены штаммы S. cerevisiae, применяющиеся в промышленности и биотехнологии.
Наряду со штаммами Петергофских генетических линий, ПГК содержит штаммы дрожжей других генетических линий, любезно предоставленные зарубежными учеными. Представляющие интерес сегреганты, полученные в результате скрещиваний этих штаммов со штаммами ПГЛ, также включены в состав коллекции. Кроме штаммов S. cerevisiae, ПГК содержит ряд штаммов других видов дрожжей, многие из которых могут быть использованы в биотехнологии.
Куратор коллекции: Анатолий Васильевич Войлоков
(тел.: (812)428-40-05, e-mail: )
Ссылки на описание коллекции:
В.Г.Смирнов, С.П.Сосниина. “Генетика ржи”. Из-во ЛГУ. 1984. 264 с.
Cайт с описанием мейотических мутантов.
Создание генетической коллекции различных форм и инбредных линий ржи Secale cereale начато в 1956 году по инициативе В.С. Федорова и продолжено в дальнейшие годы В.Г. Смирновым, С.П. Соснихиной, А.В. Войлоковым. На начальных этапах коллекцию пополняли редкие морфологические мутанты, обнаруженные в сортах ржи, и инбредные линии, получение путем прямого самоопыления самонесовместимых растений сортов. Последний прием вёл к селекции и фиксации мутаций самосовместимости (автофертильности). Таким образом была создана коллекция инбредных линий ржи, состоящая преимущественно из линий с нормальным фенотипом и различающихся по проявлению инбредной депрессии и признакам, требующим специальных методов анализа.
На основе использования автофертильных линий ржи разработан подход, позволивший за короткое время существенно пополнить коллекцию мутантными формами. Автофертильность позволила закрепить морфологические мутации при воспроизведении линий и сохранить мутации по стерильности путем поддержания в гетерозиготном состоянии.
Коллекция мутантов с разнообразным морфологическим проявлением насчитывает свыше тридцати форм и линий. В ходе проведения генетического анализа получено свыше 200 линий, сочетающих до пяти мутантных генов в одном генотипе. Для изучения молекулярно-генетических механизмов двухлокусной гаметофитной несовместимости, специфичной для злаков, создана коллекция из 100 инбредных линий, несущих независимо-выделенные мутации самосовместимости.
Для поддержания форм и линий ржи помимо индивидуальной изоляции (инбридинга) используется групповая изоляция. Большая часть генетической коллекции периодически воспроизводится. Все образцы заложены на длительное хранение. Инбредные линии ржи, а также первичные тритикале (гибриды от скрещивания пшеницы с рожью, несущие удвоенное число хромосом), полученные на основе ряда из них, представлены уникальными генотипами.
Формы с нарушением мейоза, выщепляющиеся в нескольких поколениях самоопыления, составили генетическую коллекцию мейотических мутантов ржи, которая включает 15 синаптических мутантов, 4 мутанта с нарушениями веретена, 4 мутанта с аномальной конденсацией мейотических хромосом. Подробное описание этих мутантов можно найти на сайте ryegenetics.ru.
Кураторы коллекции: Ирина Евгеньевна Додуева и Ирина Сергеевна
Бузовкина (тел. (812)328-15-90, e-mail: i.buzovkina@spbu.ru)
Ссылки на описание коллекции:
Нарбут С.И. Об изменчивости плодовитости у редиса при инцухте. Исследования по генетике. 1961. 1. с.139-146.
Нарбут С.И., Войлоков А.В., Кириллова Г.А. Генетическая характеристика линий редиса Raphanus sativus var.radicola pers. Вест.ЛГУ. 1985. 24. с. 75-78.
Рисунок 1. Пример опухолеобразования у редиса
Коллекция инбредных линий редиса (Raphanus sativus) заложена С.И. Нарбут в конце 50-х годов ХХ века путем самоопыления растений нескольких сортов. В настоящее время коллекция насчитывает около 30-ти линий разной степени фертильности. Линии отличаются от исходных сортов целым комплексом морфофизиологических признаков. Наибольший интерес представляют формы с разными типами нарушений процессов дифференцировки и морфогенеза: опухолеобразование, израстание завязи, изгибы побегов, нарушение периода покоя семян, карликовость и гигантизм растений, и др. Для ряда признаков выявлены контролирующие их гены.
Данная коллекция послужила основой пионерских работ по изучению роли генотипа в процессах дифференцировки in vitro. Сочетание генетических исследований и методов культуры органов in vitro позволило моделировать процессы нарушения морфогенеза в контролируемых условиях и доказать генетическую природу опухолеобразования (Рис. 1). На современном этапе ведутся работы по изучению роли генов, вовлеченных в системы контроля деления клеток меристем, в формировании опухолеобразования, получены трансгенные растения, несущие гены, вовлеченные в синтез и метаболизм гормонов.
Коллекция инбредных линий редиса может рассматриваться как перспективный материал для изучения регуляции разных этапов морфогенеза у высших растений, для изучения влияния инбридинга на генетическую систему строго перекрестноопыляемых растений, а также для изучения контроля хозяйственно важных признаков.
Куратор коллекции: Чекунова Елена Михайловна
(тел.: (952)376-80-35, e-mail: )
Ссылки на описание коллекции:
Квитко К.В.. Хламидомонада Chlamydomonas. “Объекты биологии развития. М., Наука, 1975, с. 13 – 22.
Квитко К.В., Борщевская Т.Н., Чунаев А.С., Тугаринов В.В. Петергофская генетическая коллекция штаммов зеленых водорослей: Chlorella, Scenedesmus, Chlamydomonas. Культивирование коллекционных штаммов водорослей. Л. ЛГУ, 1983, с. 28 – 57.
Harris E. The Chlamydomonas source book: a comprehensive guide to biology and laboratory use. Academic press, USA, 1988, 780 pp.
Рисунок 2. Пигментные мутанты C. reinhardtii из ПГК
Пигментные мутанты, находящиеся в коллекции (Рис. 2), стали источником генетического материала для изучения таких фундаментальных биологических процессов как фотосинтез, формирование мембранных структур и биосинтез хлоропластных пигментов — хлорофиллов и каротиноидов. Исследования бесхлорофилльных штаммов C. reinhardtii из этой коллекции позволили идентифицировать ряд генов (CHLH, LTS3 и SUP-I), контролирующих процессы биосинтеза хлорофилла на свету и в темноте.
Мутанты C. reinhardtii, дефектные по гену CHLH, послужили основой для создания штаммов-продуцентов химически-чистого протопорфирина IX (ПП). ПП — биосинтетический предшественник хлорофилла, который является сильным фотосенсибилизатором. Его используют в целях флуоресцентной диагностики канцерогенеза и при фотодинамической терапии, при создании порфирин-содержащих полимеров — основных компонентов сенсоров, позволяющих выявлять широкий спектр токсичных элементов в окружающей среде.
Таким образом, мутанты из ПГК не только позволяют осуществлять фундаментальные исследования в области генетики фотосинтеза, но и являются источником материала для проведения актуальных прикладных исследований в медицине, экологии, фотобиологии и энергетике. Коллекция также представляет богатый материал для проведения учебных и практических занятий.

199034, Санкт-Петербург, Университетская наб., 7-9
© Санкт-Петербургский государственный университет, 2006-2017