ГАЗОВЫЕ СМЕСИ. ТЕПЛОЕМКОСТЬ
Газовые смеси
Газовая смесь представляет собой смесь газов, химически не взаимодействующих между собой. Простейшим представителем газовых смесей является воздух, который состоит из кислорода, азота, водяных паров, метана, ксенона, гелия и других газов. В результате процесса горения топлива также получается газовая смесь. Состав этой смеси, или продуктов сгорания топлива, может быть самым разнообразным и зависит как от состава топлива, так и от условий, при которых происходит процесс сгорания (в частности, от количества подводимого воздуха).
Газовые смеси рассматриваются как идеальные газы и подчиняются законам идеальных газов. Уравнением состояния для них служит уравнение Менделеева — Клапейрона.
Для определения величин, характеризующих газовую смесь, необходимо знать состав газа. Он определяется количеством каждого из газов, входящих в смесь, и задается по массе или объему. Если, например, смесь состоит из трех газов и масса каждого из них Мь М2 и М3, то доли каждого из газов т1> т2 и т3, определяющие относительный массовый состав, выразятся так:
Если смесь состоит из п газов, то для любого из них массовая доля составляет
Таким образом, массовой долей компонента называется отношение массы компонента к массе смеси.
Сумма массовых долей компонентов равна единице:
где индекс /с относится к каждому отдельному газу, входящему в смесь.
Известно, что газ не имеет своего объема и объем газа занимает объем того сосуда, в котором движутся молекулы газа (рис. 2.1).
Рис. 2.1. Распределение молекул газа
Молекулы каждого газа, входящего в смесь, равномерно распределены по всему объему, так что каждый из газов, составляющих смесь, занимает такой же объем, как и вся смесь. При этом каждый из газов оказывает на стенки сосудов некоторое давление, называемое парциальным давлением. Таким образом, занимая объем, равный объему смеси, каждый из газов, составляющих смесь, находится под своим парциальным давлением и имеет температуру смеси. Вся же смесь идеальных газов оказывает на стенки сосуда давление, равное сумме парциальных давлений. Это положение называется законом Дальтона. Джон Дальтон (англ. John Dalton, 1766—1844) — английский химик и физик. Он сформулировал (1803) закон парциальных давлений газов, ввел понятие «атомный вес», первым определил атомные веса (массы) ряда элементов. Также он первым (1794) описал дефект зрения, которым страдал сам, позже названный дальтонизмом.
Математическое выражение этого закона записывается так:
Для установления объемной доли компонента вводится понятие парциального объема компонента, под которым принимается такой его объем, который он занимал бы при температуре и давлении смеси, и тогда под объемной долей компонента гк понимают отношение
где каждый из объемов представляет собой не действительный объем газа, входящего в смесь, а парциальный объем. Так как каждый из газов, составляющих смесь, имеет температуру смеси, то для вычисления парциального объема можно воспользоваться законом Бойля — Мариотта:
где рг, р2, рк, рп — парциальные давления; V1> V2, Vk, Vn — парциальные объемы; Усм — объем всей смеси; р — давление смеси. Складывая почленно написанные уравнения, получаем:
В левой части в скобках сумма парциальных давлений смеси, которая равна р смеси. Сокращая, получаем:
т. е. сумма парциальных объемов равна объему смеси. На основании формулы (2.4) получаем:
Таким образом, объемная доля каждого газа, входящего в состав смеси, равна отношению его парциального объема к объему всей смеси. При этом сумма объемных долей компонентов равна единице:
Если известны масса газа М и его молекулярная масса ц, то число киломолей к этого газа определится из соотношения
Количество киломолей смеси равно сумме киломолей компонентов смеси, т. е.
Пользуясь величиной ксм, можно ввести понятие киломолъ смеси по зависимости
Эта величина измеряется в кг/кмоль; численно равная ей отвлеченная величина, также обозначаемая рсм, называется средней молекулярной массой. Эта величина вводится для удобства при расчетах.
Молекулярная масса смеси газов определяется по формуле
Таким образом, молекулярная масса смеси представляет собой сумму молекулярных масс всех компонентов, взятых в той объемной доле, в которой компонент входит в смесь.
Смеси идеальных газов подчиняются тем же законам, что и отдельные идеальные газы. Следует только иметь в виду, что в формулы для решения задач подставляются значения молекулярной массы смеси, газовой постоянной смеси, объема и давления смеси. Для решения задач, связанных с расчетом газовых смесей, используются формулы, приведенные в табл. 2.1.
Определение температуры смеси.
В технике часто приходится иметь дело с объектами или процессами, в которых смешиваются два или более потоков. Потоки могут состоять из разных веществ в разных агрегатных состояниях, иметь разные давления и температуры (например, смешивание воды и пара). Для лучшего перемешивания иногда используется перемешивающее устройство. В частности, для системы, изображенной на рис. 3.15, балансы массы и энергии можно записать так:
Рис. 3.15. Перемешивающее устройство
Пренебрегая изменением кинетической и потенциальной энергии, запишем
Если перемешивание происходит без теплообмена с окружающей средой и без совершения работы, то это выражение упрощается:
Это соотношение можно представить в виде
или, полагая, что теплоемкости постоянны,
Таким образом, зная температуры и потоки масс компонентов на входе, можно определить стационарную температуру потока на выходе.
Например, если два вещества с температурами tx и t2, с потоками масс щ, т2 и удельными теплоемкостями ср <ср2 соответственно смешиваются при постоянном давлении, то приближенное значение температуры смеси можно найти по формуле
Если система состоит из нескольких таких фрагментов, то ее равновесную температуру приближенно можно рассчитать по формуле
Если выравнивание температур происходит при постоянном объеме, без теплообмена и совершения работы, то баланс энергии в стационарном режиме можно представить в виде равенства
где Е <— энергия компонентов до смешения; Е2 — энергия после смешения,
В общем случае выполняется равенство
Если известны теплоемкости, температуры и массы компонентов, можно найти приближенное значение равновесной температуры смеси, полагая, что теплоемкости всех компонентов постоянны или используя средние значения теплоемкостей. Расчет температуры смеси в этом случае производится по формуле
В калориметре с адиабатными стенками находится mw = 800 г воды при температуре tw = 15°С, теплоемкость воды cw = 4,19 кДж/ (кг-К). Вода находится в серебряном стакане массой ms = 250 г, теплоемкость серебра cs = 0,23 кДж/ (кг-К). В воду бросают кусок алюминия массой тА = 200 г с температурой tA = 100°С. После выравнивания температур температура системы равна tm = 19,2°С. Чему равна теплоемкость алюминия?
Рассмотрим еще один пример.
Баланс энергии для стационарного режима работы

В стационарном режиме суммарный поток энергии из холодильника в окружающую среду равен потребляемой мощности. При этом изменение внутренней энергии воздуха в единицу времени равно
Как узнать температуру смеси газов
В практической деятельности чаще всего имеют дело не с однородными газами, а с их смесями: воздух, продукты сгорания топлива, горючие газовые смеси и т.п.. Поэтому в теплотехнике газовые смеси имеют важное значение.
В объеме, занимаемом газовой смесью, каждый газ, входящий в эту смесь, ведет себя так же, как он вел бы себя при отсутствии других составляющих смеси: распространяется по всему объему; создает давление (парциальное), определяемое температурой и объемом на единицу его массы; имеет температуру смеси.
Смесь идеальных газов представляет собой идеальный газ, для которого справедливы законы и полученные для идеальных газов зависимости.
Для идеального газа давление определяется выражением (4.1)
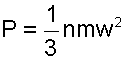 |
Количество молекул, входящих в данную смесь газов, равно сумме молекул газов, составляющих смесь
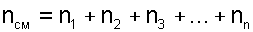 |
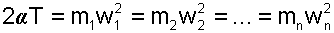 |
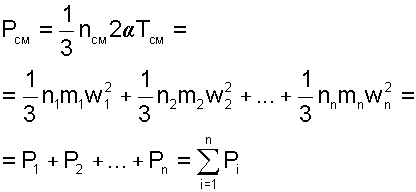 |
где Pi— парциальные давления газов, составляющих смесь.
Уравнение (4.65) представляет математическое выражение закона Дальтона (1807 г.), в соответствии с которым, давление газовой смеси равно сумме парциальных давлений газов, входящих в смесь. Парциальное давление это давление, которое создает один из газов, составляющих смесь, при температуре смеси в случае заполнения им всего объема смеси. Парциальное давление это реальносуществующая величина, поскольку каждый отдельный газ в смеси имеет температуру смеси и занимает весь объем смеси. Парциальное давление можно определить из уравнения Менделеева-Клапейрона
Как узнать температуру смеси газов
Смешение в объёме – это смешение веществ (газов, паров, жидкостей) за счёт их взаимного диффузионного проникновения после удаления (разрушения) разделяющих их непроницаемых перегородок и без изменения суммарного объёма веществ.
Допустим, что в двух отсеках сосуда (рис. 6.1) объёмом V, разделённого адиабатной перегородкой, находятся разные газы при разных давлениях и температурах.
 |
а объём – сумме первоначальных объёмов этих газов
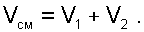 |
В результате удельный объём смеси двух или более компонентов газов будет, определятся как:
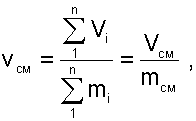 |
где n – число смешивающихся компонентов газа.
Для определения параметров состояния смеси газов, с известным массовым составом и известными параметрами газов до смешения, необходимо знать ещё один параметр. Он определяется на основании первого закона термодинамики для данной системы
 |
При адиабатном смешении газов без изменения общего объёма сосуда, теплота и работа изменения объема равны нулю (Q=0, L=0). Следовательно, изменения внутренней энергии в системе нет, т.е. внутренняя энергия после смешения равна сумме внутренних энергий компонентов смеси до смешения:
 |
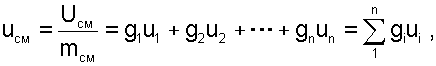 |
где gi=mi/mСМ – массовые доли компонентов смеси газов.
Удельный объём (vСМ) и удельная внутренняя энергия (uСМ) при известном составе смеси, определяет состояние смеси. По ним могут быть найдены остальные параметры смеси. Для реальных газов они обычно определяются по таблицам термодинамических свойств веществ.
Для идеальных газов внутренняя энергия функция только температуры, и поэтому задача определения параметров смеси упрощается. Приняв начало отсчёта внутренней энергии при 0 О C и, считая постоянной изохорную теплоемкость идеальных газов, можно записать:
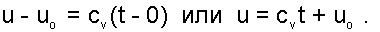 |
 |
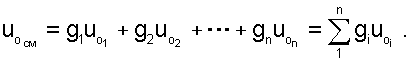 |
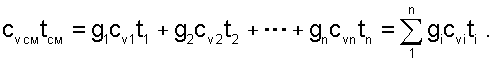 |
 |
получим из уравнения (6.7) расчётное выражение для температуры смеси идеальных газов:
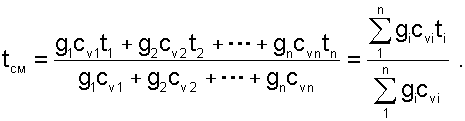 |
 |
Изменение энтропии системы в расчёте на один килограмм смеси определяется как сумма изменений энтропий компонентов смеси газа:
 |
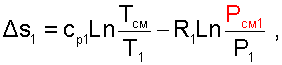 |
где – РСМ1 парциальное давление первого компонента смеси газа при температуре смеси, когда этот газ занимает весь объем и соответствует выражению
 |
Потери потенциальновозможной полезной работы газа (эксергии) в этом необратимом процессе ведутся традиционно по теореме Гюи-Стодолы [1]:
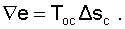 |
Используя выражения 6.1-6.8 можно решить и обратную задачу – нахождения масс или массовых долей компонентов смеси данных газов при известных их начальных параметрах, необходимых для получения необходимых параметров смеси газов.
Определение температуры газовых смесей



Методические указания
К выполнению курсовой и расчетной работы
По курсу
„ Теория сжигания и топливосжигающие устройства ”

Донецкий национальный технический университет
Кафедра промышленной теплоэнергетики
к выполнению курсовой и расчетной работы
„ Теория сжигания и топливосжигающие устройства ”
для студентов очной и заочной формы обучения
7.090521 «Тепловые электрические станции»
7.000008 «Энергетический менеджмент»
на заседании кафедры
протокол № ___ от «___» _____________2006 г.
на заседании учебно-издательского совета ДонНТУ
протокол № ___ от «___» ____________ 2006 г.
Донецк, ДонНТУ, 2005
 |
Приведены методика и основные расчетные формулы, диаграммы и табличные данные для выполнения студентами курсовой работы по дисциплине „ Теория сжигания и топливосжигающие устройства ”.
Составители : С.М. Сафьянц, проф.
Отв. за выпуск Е.К. Сафонова, доц.
ã Сафьянц С.М., Попов А.Л., Сафонова Е.К., Безбородов Д.Л. Петров А.В.
ã Донецкий национальный технический университет, 2006 г.
1 ОПРЕДЕЛЕНИЕ ТЕПЛОТА СГОРАНИЯ ГАЗООБРАЗНОГО ТОПЛИВА
Теплоту сгорания газообразного топлива можно рассчитать, если известны тепловые эффекты реакций горения (табл. 1) и химический состав топлива [в % (объемн.)].
Теплота сгорания топлива
Так, например, низшую объемную теплоту сгорания газообразного топлива в кДж (ккал) подсчитывают по следующим формулам:
где 127,7; 30,5 – тепло, выделяемое при сгорании 1% (объемн.) СО, кДж (ккал);
108; 25,8 – аналогичные величины для Н2 … и т. д.;
СО, Н2, СН4 … и т. д. – содержание горючих составляющих топлива, % (объемн.).
В формуле (1) соответствующие тепловые эффекты выражены в килоджоулях.
Следует отметить, что расчетная величина теплоты сгорания может немного отличаться от опытной, так как в газе содержатся пыль и смолы.
Пример 1. Определить низшую объемную теплоту сгорания природного газа, состав которого дан, по формуле (1) :
Q υ н = 358 ∙ 88,69 + 636 ∙ 3,92 + 913 ∙ 0,9 + 1465 ∙ 0,46 = 36200 кдж/м 3 (8640 ккал/м 3 ).
Теплота сгорания твердого и жидкого топлив
Нахождение теплоты сгорания твердого и жидкого топлив расчетным способом носит приближенный характер, так как это топливо анализируют не по химическим соединениям, а лишь по химическим элементам.

Д. И. Менделеев предложил следующую формулу;
В пересчете на килоджоули формула принимает вид:
Q р в = 340 С р + 1260 Н р – 109 (О р – S р ) кДж/кг, (2)
Q р в = 81 С р + 300 Н р – 26 (О р –S р ) ккал /кг, (2 а)
Высшую теплоту сгорания водорода, входящего в состав органических соединений, Менделеев принял равной 126 МДж/кг (30000 ккал/кг), а не фактическую высшую теплоту сгорания 142 МДж/кг (34180 ккал/кг). Снижение теплоты сгорания топлива из-за наличия в горючей массе кислорода учтено коэффициентом 26, полученном из опытов. Этот коэффициент показывает, что каждый процент по массе кислорода в топливе снижает теплоту сгорания топлива на 109 кдж (26 ккал). Теплота сгорания серы, по Менделееву, принята равной 10,9 МДж/кг (2600 ккал/кг).
На основании формулы (2) формула Менделеева для определения низшей массовой теплоты сгорания топлива принимает вид:
где W – содержание влаги в топливе, % по массе.
Формула Менделеева пригодна для всех видов твердого и жидкого топлив.
Из других топлив формул для подсчета теплоты сгорания следует отметить формулы Гуталя и Коновалова.
Формула Гуталя дает возможность рассчитать приближенно теплоту сгорания каменного угля по данным технического анализа:
Qв = 82 
где 82 – теплота сгорания 1% по массе С, принятая Гуталем;

V г – выход летучих, отнесенных к горючей массе топлива, % по массе;
Этот коэффициент по существу представляет собой 1% теплоты сгорания горючей массы летучих топлива, кДж (ккал).
Формула Коновалова имеет вид

А – значение теплоты сгорания, отнесенной к 1 кг кислорода при полном сжигании топлива.
Из табл. 1 видно, что значения А для различных горючих элементов колеблются в узких пределах, так например, значение А для углерода и водорода соответственно равно 12,77 и 15,11 МДж/кг, в то время как теплота сгорания этих элементов отличается примерно в 4 раза (34,1 и 121 Мдж/кг).
На этом основании и построена формула Коновалова. Коэффициент А для каменного угля и нефти принимают равным 12,77 МДж/кг (3050 ккал/кг), для торфа 13,2 МДж/кг (3150 ккал/кг) и для дров 13,6 МДж/кг (3250 ккал/кг).
Принцип подсчета коэффициента А определен на примере горения окиси углерода (СО + 0,5О2 = СО2):
А = 

2. РАСХОД КИСЛОРОДА ДЛЯ ГОРЕНИЯ ТОПЛИВА
Количество кислорода (кг), которое необходимо израсходовать для полного сгорания единицы топлива (1 кг), согласно стехиометрическому соотношению, в химической реакции горения называется удельным теоретическим расходом кислорода. Это стехиометрическое число ωо, кг/кг, зависит:
1) от природы горючих элементов топлива:
для окиси углерода:
Углеводороды имеют значения ωо, близкие к углероду (табл. 2), так как масса водорода в углеводородах невелика;
2) от концентрации горючих элементов в техническом топливе, чем больше балласта в топливе, тем меньше ωо.
Теоретический расход кислорода и атмосферного воздуха
на единицу топлива
| Название горючих топлив | Состав | Реакция горения | Расход кислорода | Расход воздуха | |||
| ωо | V  | L  | |||||
| Кг/кг | М 3 /кг | М 3 /м 3 | М 3 /кг | М 3 /м 3 | |||
| Углерод | С | С+О2=СО2 | 2,667 | 1,867 | — | 8,89 | — |
| Окись углерода | СО | СО+0,5О2=СО2 | 0,572 | 0,40 | 0,5 | 1,90 | 2,38 |
| Водород | Н2 | Н2+0,5О2=Н2О | 5,60 | 0,5 | 26,74 | 2,38 | |
| Сера | S | S+O2=SO2 | 0.7 | — | 3.33 | — | |
| Метан | СН4 | СН4+2О2=СО2+2Н2О | 2,80 | 13,31 | 9,52 | ||
| Этан | С2Н6 | С2Н6+3,5О2=2СО2+3Н2О | 3,74 | 2,60 | 3,5 | 12,43 | 16,66 |
| Пропан | С3Н8 | С3Н8+5О2=3СО2+4Н2О | 3,64 | 2,54 | 12,10 | 23,80 | |
| Бутан | С4Н10 | С4Н10+6,5О2=4СО2+5Н2О | 3,58 | 2,50 | 6,5 | 11,90 | 30,94 |
| Пентан | С5Н12 | С5Н12+8О2=5СО2+6Н2О | 3,56 | 2,49 | 11,85 | 38,08 | |
| Циклогексан | С6Н12 | С6Н12+9О2=6СО2+6Н2О | 3,43 | 2,40 | 11,42 | 42,71 | |
| Этилен | С2Н4 | С2Н4+3О2=2СО2+2Н2О | 3,04 | 2,13 | 1,5 | 10,26 | 11,90 |
| Бензол | С6Н6 | С6Н6+7,5О2=6СО2+3Н2О | 3,0 | 2,10 | 7,5 | 12,4 | 35,70 |
| Сероводород | Н2S | Н2S+1,5О2=Н2О+О2 | 1,41 | 0,98 | 1,5 | 4,73 | 7,14 |
При наличии многих горючих составляющих в топливе стехиометрическое число
ωо = 0,01∑wxc 
где wx – стехиометрическое число соответствующего горючего, кг/кг;
c 
После подстановки значений ωс, ωН и ωS из табл. (2) получаем следующую формулу:
ωо = 0,01(2,667С р + 8Н р + S р – О р ) кг/кг. (9 а)
Теоретический объемный расход О2 (V 
V 

где ρ 
Например для углерода
V 

Значения V 
V 

Или после подстановки ωС, ωН из табл. 2
В случае расчета V 
При расчете теоретического расхода кислорода, необходимого для полного сгорания 1 м 3 газообразного топлива, нужно V 
Формула (11) путем простых преобразований может быть приведена к виду
где V 
c 
Стехиометрические объемные соотношения в реакции горения равны отношению молей. Так, для сгорания 1 м 3 СО по реакции горения требуется V 
Пользуясь этими данными и зная состав газообразного топлива в объемных процентах, определяем V 
Если обозначить углеводороды через СmHn, то количество кислорода, рекомендуемое для полного сгорания всех углеводородов, может быть представлено общей формулой
Например, для горения 1 м 3 этана С2Н6, когда m = 2 и n = 6,
Тогда в общем виде формула (13) примет вид
3. РАСХОД ВОЗДУХА ДЛЯ ГОРЕНИЯ ТОПЛИВА.
КОЭФФИЦИЕНТ РАСХОДА ВОЗДУХА
Количество воздуха, необходимого для горения топлива, можно определять по объему (м 3 ) или по массе (кг). Расход воздуха, отвечающий стехиометрическому, также называется теоретическим. Объемный расход воздуха обозначают Lо (м 3 /кг, м 3 /м 3 ), а расход по массе Gо (кг/кг). Для расчета воздуха на горение существуют три метода: аналитический, приближенный, по графикам.
Аналитический метод расчета. Теоретический расход воздуха определяют по теоретическому расходу кислорода [формулы (11 – 13)] и объемной доле кислорода в воздухе k 
Подставив V 
L 

Для атмосферного воздуха k 
Объемный теоретический расход сухого воздуха на 1 м 3 газообразного топлива определится по формуле (16):
Для атмосферного воздуха k 
Коэффициенты, показывающие теоретический расход сухого атмосферного воздуха (м 3 ) на 1 м 3 соответствующего горючего, приведены в табл. (2).
L 

Чтобы обеспечить более быстрое и полное сгорание топлива, вводят избыточный воздух в некотором количестве сверх теоретического L 


α= 

Так как избыточный воздух переходит в продукты сгорания, увеличивая их объем, и тем самым повышает унос тепла с отходящими газами, то стремятся осуществить сжигание топлива при минимальном избытке воздуха, обеспечивающем полноту сгорания в данном конкретном случае. Чем лучше организация сжигания топлива, тем меньше избытка воздуха требуется. Ориентировочные нормы коэффициента избытка воздуха, которые могут изменяться в зависимости от организации процесса сжигания топлива (от конструкции горелок и форсунок), колеблются на практике в следующих пределах: для газообразных топлив α=0,03÷0,15, для жидких топлив α=0,15÷0,20.
Воздух в количестве, которое практически вводят для полного сгорания единицы топлива, называют д е й с т в и т е л ь н ы м р а с х о д о м воздуха (L 





следовательно, L 

Приближенный метод расчета. Нужно отметить следующую закономерность: чем больше теплота сгорания топлива (Q 
L 

где k – поправочный коэффициент, зависящий от рода топлива, значение которого приведено в табл. (3) (значение его близко к единице; для углерода его значение максимально k = 1,10, для окиси углерода – минимально k = 0,788, для водорода k = 0,93).
Значение коэффициента k в формуле (21)
| Вид топлива | Коэффициент k |
| Водород | 0,93 |
| Углерод | 1,10 |
| Антрацит | 1,10 |
| Угли | 1,10 |
| Жидкое топливо | 1,10 |
| Природный газ | 1,11 |
| Метан | 1,11 |
| Торф | 1,10 |
| Дрова | 1,06 |
| Коксовый газ | 1,02 |
| Окись углерода | 0,788 |
| Доменный газ | 0,81 |
| Генераторный газ | 0,87 |
В формуле (21) Q 
Для быстрого и ориентировочного определения расхода воздуха можно исходить из положения, что на 1000 ккал теплоты сгорания топлива требуется приблизительно 1 м 3 воздуха. Лучшее приближение получается по формулам, приведенным в табл. 4.
Эмпирические формулы для определения L 

1. Объем углекислого газа
V 
где 1,867 – объем углекислого газа, полученный при полном сгорании 1 кг углерода.
2. Объем водяных паров складывается:
а) из объема водяных паров, образовавшихся от сгорания 1 кмоля водорода топлива в количестве 22,4:2=11,2 м3/кмоль;
б) из объема водяных паров, полученных в результате испарения влаги топлива – 1,242 Wр, где 1,242 – удельный объем водяного пара (м3/кг);
в) при сжигании жидкого топлива его предварительно распыляют воздухом или паром; если обозначить через Wф количество пара (в килограммах), расходуемое в форсунках для распыления 100 кг топлива, то количество пара в продуктах сгорания увеличится на 1,242 Wф (м3/кг);
г) из объема водяных паров, перешедших из воздуха: 0,00124fL 
Общее количество водяных паров в продуктах сгорания
V 

При наличии серы в продуктах сгорания будет присутствовать сернистый газ. Из 1 кг S получится 22,4:32 = 0,7 м 3 SО2.
V 


= 0,01∙1,867(С р +0,375S р ) м3/кг (24)
Следовательно, объем азота в продуктах сгорания
5. Объем избыточного кислорода воздуха
V 


Общий объем продуктов сгорания (V д ) при сжигании твердого и жидкого топлива
V д = 0,01(1,867С р +0,7S р )+0,01[11,2Н р +1,242(W p +Wф)] + 0,00124f в L 
При сжигании газообразного топлива объем продуктов сгорания определяют по следующим формулам:
1. Объем углекислого газа:
где CO 
Из 1 м 3 СО получается 1 м 3 СО2, поэтому при окиси углерода стоит коэффициент 1. При горении углеводородов CmHn количество молей СО2 в реакции получается равным количеству атомов углерода. Например, при горении С2Н6 получается 2СО2 и т. д.
Общая формула для подсчета объема углекислого газа, полученного при полном сгорании углеводородов CmHn:
V 
Аналогично подсчитывают объем водяного пара, полученного при полном сгорании CmHn:
V 

2. Объем водяного пара
5. Объем избыточного кислорода:
Общий объем продуктов горения:
V д = 0,01[СО 






Определение температуры газовых смесей
Температуру газовых смесей можно определить по правилу смещения. Таким образом, сумма теплосодержаний отдельных компонентов до смешения должна быть равна общему теплосодержанию смеси, если при смешении не происходит никаких химических реакций. В этом случае компоненты могут и не принадлежать к различным газам, а лишь иметь различную начальную температуру.

В левой части равенства сумма слагаемых представляет собой количество тепла, заключающееся в смеси, в правой — каждое слагаемое есть количество тепла, вносимое каждым компонентом.
Из этого равенства следует, что

Трудность решения задачи заключается в том, что присутствующие в правой части равенства величины с1‘,с2‘, c3‘. суть функции от неизвестной, подлежащей определению величины t. Приближенное решение достигается одним из следующих способов.
Второй способ приближенного решения задачи заключается в следующем. В равенстве

заменим произведения с‘t через i так, чтобы


Стоящая в правой части сумма Sui задана.
При решении задачи поступаем так. Задаемся каким-либо значением (t)1; для него подсчитываем S(ui‘)1 и сравниваем суммой Sui. Если S(ui‘) соответствующая (t)1 больше заданной Sui, то, следовательно, (t) выбрана выше истинной. Выбираем второе значение для t- (t)2 и для него находим сумму S(ui‘)2. Если при этом
то искомая температура лежит между значениями (t)1 и (t)2.
Выбирая значения (t)1 и (t)2 так, чтобы разность (t)1 — (t)2 была возможно меньшей (практически 50° или 100°), можно истинное значение (t) найти путем интерполяции в этих пределах.
Повышению температуры смеси на (t)1—(t)2=100° соответствует увеличение количества, содержащегося в смеси тепла на q1—q2.
Очевидно, что искомому увеличению температуры смеси t-(t)2 =х 0 соответствует изменение количества тепла, равное q—q2 из четырех величин 100, (q1—q2), x и (q — q2) составляем пропорцию, основываясь на предположении, что в интервале (t)1 и (t)2 теплоемкость постоянна. Тогда
Эти весьма важные для определения температуры смеси газов методы поясним примерами.
Пример 1. К 1 нм 3 продуктов сгорания топлива, содержащих 14,0% СO2; 5,5% H2O; 4,1% О2 и 76,4% N2 примешивается 0,5 м 3 воздуха, Определить температуру смеси, если начальная температура продуктов сгорания 1000° и воздуха 50°.
Пользуясь первым из изложенных методов, имеем (уравнение 2):
При этой температуре
Последнее значение удовлетворительно, так как дальнейшие уточнения дадут изменение температуры менее чем на 2—3°,
Пример 2. Теплосодержание 1 нм 3 продуктов сгорания торфа равно 750 ккал. Определить соответствующую данному теплосодержанию температуру, если состав продуктов сгорания по объему следующий: 16,0% СО2; 17,4% H2O; 66,6% N2
Пользуясь для решения этой задачи вторым методом, имеем:
Задаемся (t)1= 1900°. Для этой температуры
Следовательно,
Искомая температура весьма просто может быть определена по формуле:
Принимая значение с средней теплоемкости продуктов сгорания торфа равным 0,41, определяем искомую температуру продуктом сгорания:
























































