Синдром вертебральной артерии
Синдром вертебральной артерии
Учитывая, что причиной синдрома могут различные факторы, иногда возникают трудности с трактовкой такого диагноза, как синдром вертебральной артерии, так как этим синдромом можно обозначить самые различные состояния, например, такие как острые нарушения кровообращения. Но в клинической практике наибольше значение имеют дегенеративно-дистрофические изменения в шейном отделе позвоночника и аномальные явления со стороны атланта, которые приводят к нарушению кровотока в бассейне вертебральных артерий и появлению симптомов нарушения мозгового кровообращения.
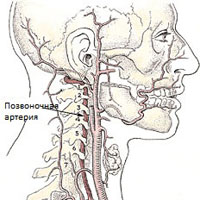
Различают экстракраниальный и интракраниальный отделы позвоночной артерии.
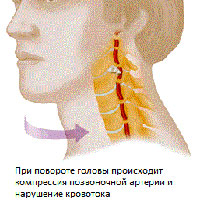
Значительная часть экстракраниального отдела позвоночные артерии проходят через подвижный канал образованный отверстиями в поперечных отростках позвонков. Через этот канал проходит также симпатический нерв (нерв Франка). На уровне С1-С2 позвоночные артерии закрываются только мягкими тканями. Такая анатомическая особенность прохождения позвоночных артерий и мобильность шейного отдела значительно увеличивают риск развития компрессионного воздействия на сосуды со стороны окружающих тканей.
Возникающая компрессия со стороны окружающих тканей приводит к компрессии артерии вегетативных окончаний и констрикции сосудов вследствие рефлекторного спазма, что приводит к недостаточному кровоснабжению головного мозга.
Дегенеративные изменения в шейном отделе (остеохондроз, артроз фасеточных суставов, унковертебральный артроз, нестабильность двигательных сегментов, грыжи дисков, деформирующий спондилез, костные разрастания (остеофиты), мышечные рефлекторные синдромы (синдром нижней косой мышцы, синдром передней лестничной мышцы)- являются нередко причиной компрессии позвоночный артерий и развития синдрома вертебральной артерии. Чаще всего, компрессия возникает на уровне 5-6 позвонков, чуть реже на уровне 4-5 и 6-7 позвонков. Наиболее частой причиной развития синдрома позвоночной артерии является унковертебральный синдром. Близкое расположение этих сочленений к позвоночным артериям приводит к тому, что даже небольшие экзостозы в области унковертебральных сочленений приводят к механическому воздействию на позвоночные артерии. При значительных унковертебральных экзостозах возможно значительное сдавление просвета вертебральных артерий.
Достаточно значимую роль в развитии синдрома вертебральной артерии играют аномалии Кимберли, Пауэрса.
Симптомы
По клиническому течению различают две стадии синдрома вертебральной артерии функциональную и органическую.
Для функциональной стадии синдрома вертебральной артерии характерна определенная группа симптомов: головные боли с некоторыми вегетативными нарушениями кохлеовестибулярные и зрительные нарушения. Головная боль может иметь различные формы, как острая пульсирующая, так и ноющая постоянная или резко усиливающаяся особенно при поворотах головы или длительных статической нагрузке. Головная боль может распространяться от затылка ко лбу. Нарушения в кохлеовестибулярной системе могут проявляться головокружением пароксизмального характера (неустойчивость покачивание) или системного головокружения. Кроме того, возможно некоторое снижение слуха. Нарушения зрительного плана могут проявляться потемнением в глазах, ощущением искр, песка в глазах.
По типу гемодинамических нарушений различают несколько вариантов синдрома позвоночной артерии (компрессионная, ирритативная, ангиоспатическая и смешанная формы).
Сужение сосуда при компрессионном варианте происходит вследствие механической компрессии на стенку артерии. При ирритативном типе синдром развивается вследствие рефлекторного спазмам сосуда из-за ирритации симпатических волокон. В клинике, чаще всего, встречаются комбинированные (компрессионно-ирритативные) варианты синдрома позвоночной артерии. При ангиоспастическом варианте синдрома также имеется рефлекторный механизм, но возникает от раздражения рецепторов в области двигательных сегментов шейного отдела позвоночника. При ангиоспастическим варианте преобладают вегето-сосудистые нарушения и симптоматика не так сильно обусловлена с поворотами головы.
Клинические типы синдрома
Заднешейный симпатический синдром (Барре – Льеу)
Задне-шейный синдром характеризуется головными болями с локализацией в шейно-затылочной области с иррадиацией в переднюю часть головы. Головная боль, как правило, постоянная нередко по утрам особенно после сна на неудобной подушке. Головная боль может при ходьбе, езде на автомобиле, при движениях в шее. Головная боль также может быть пульсирующей, прокалывающей с локализацией в шейно-затылочной области и с иррадиацией в теменную лобную и височную зоны. Головная боль может усиливаться при поворотах головы и сопровождается как вестибулярными, так и зрительными и вегетативными нарушениями.
Мигрень базилярная
Базилярная мигрень возникает не в результате компрессии вертебральной артерии, а вследствие стеноза вертебральной артерии, но клинически имеет много общего с другими формами синдрома позвоночной артерии. Как правило, мигренозный приступ начинается с резкой головной боли в области затылка, рвотой, иногда с потерей сознания. Возможны также зрительные нарушения, головокружение, дизартрия, атаксия.
Вестибуло – кохлеарный синдром
Нарушения со стороны слухового аппарата проявляются в виде шума в голове, снижения восприятия шепотной речи и фиксируются изменениями данных при аудиометрии. Шум в ушах имеет стойкий и продолжительный характер и тенденцию к изменению характера при движении головы. Кохлеарные нарушения ассоциированы с головокружениями (как системными, так и несистемными).
Офтальмический синдром
При офтальмическом синдроме на первом плане зрительные нарушения, такие как мерцательная скотома, снижение зрения фотопсия могут также быть симптомы конъюнктивита (слезотечение гиперемия конъюнктивы). Выпадение полей зрения может быть эпизодическим и в основном связаны с изменением положения головы.
Синдром вегетативных изменений
Как правило, вегетативные нарушения не проявляются изолированно, а сочетаются с одним из синдромов. Вегетативные симптомы, как правило, следующие: ощущение жара, чувство похолодания конечностей, потливость, изменения кожного дермографизма, нарушения сна.
Преходящие (транзиторные) ишемические атаки
Ишемические атаки могут иметь место при ишемической стадии синдрома вертебральной артерии. Наиболее частыми симптомами таких атак являются: преходящие моторные и чувствительные нарушения, нарушения зрения, гемианопсия, атаксия, приступы головокружения, тошнота, рвота, нарушение речи, глотания, двоение в глазах.
Синкопальный вертебральной синдром (Синдром Унтерхарншайта)
Эпизод синкопального вертебрального синдрома представляет собой острое нарушение кровообращения в области ретикулярной формации мозга. Этот эпизод характеризуется краткосрочным отключением сознания при резком повороте головы.
Эпизоды дроп-атаки
Эпизод дроп-атаки (падения) обусловлен нарушением кровообращения в каудальных отделах ствола мозга и мозжечка и клинически будет проявляться тетраплегией при запрокидывании головы. Восстановление двигательных функций достаточно быстро.
Диагностика
Диагностика синдрома вертебральной артерии представляет определенные сложности и Нередко происходит как гипердиагностика, так и гиподиагностика синдрома вертебральной артерии. Гипердиагностика синдрома часто обусловлена недостаточным обследованием пациентов особенно при наличии вестибуло-атактического и/или кохлеарного синдрома, когда врачу не удается диагностировать заболевания лабиринта.
Для установления диагноза синдрома позвоночной артерии необходимо наличие 3 критериев.
Лечение
Лечение синдрома вертебральной (позвоночной) артерии состоит из двух основных направлений: улучшение гемодинамики и лечение заболеваний приведших к компрессии позвоночных артерий.
Медикаментозное лечение
Противовоспалительная и противоотечная терапия направлена на уменьшение периваскулярного отека возникающего из-за механической компрессии. Препараты, регулирующие венозный отток (троксерутин, гинко-билоба, диосмин). НПВС (целебрекс, лорноксикам, целекоксиб)
Сосудистая терапия направлена на улучшение кровообращения головного мозга, так как нарушения гемодинамики имеют место у 100% пациентов с этим синдромом. Современные методы диагностики позволяют оценить эффективность лечения этими препаратами и динамику кровотока в сосудах головного мозга с помощью УЗИ исследования. Для сосудистой терапии применяются следующие препараты: производные пурина (трентал) производные барвинка (винкамин,винпоцетин) антагонисты кальция (нимодипин) альфа-адреноблокаторы (ницерголин) инстенон сермион.
Нейропротективная терапия
Одно из самых современных направлений медикаментозного лечения является применение препаратов для улучшения энергических процессов в головном мозге, что позволяет минимизировать повреждение нейронов вследствие эпизодических нарушений кровообращения. К нейропротекторам относятся: холинергические препараты (цитиколин, глиатилин), препараты улучшающие регенерацию (актовегин, церебролизин), нооотропы (пирацетам, мексидол), метаболическая терапия (милдронат, Тиотриазолин, Триметазидин)
Симптоматическая терапия включает использование таких препаратов, как миорелаксанты, антимигренозные препараты, антигистаминные и другие.
Лечение дегенеративных заболеваний включает в себя немедикаментозные методы лечения, такие как ЛФК, физиотерапия, массаж, иглотерапия, мануальная терапия.
В большинстве случаев применение комплексного лечения включающего как медикаментозное, так и немедикаментозное лечение, позволяет добиться снижения симптоматики и улучшить кровообращение головного мозга.
Хирургические методы лечения применяются в тех случаях, когда имеется выраженная компрессия артерий (грыжей диска, остеофитом) и только оперативная декомпрессия позволяет добиться клинического результата.
Использование материалов допускается при указании активной гиперссылки на постоянную страницу статьи.
Кохлеарный неврит слухового нерва причины, симптомы, методы лечения и профилактики
Кохлеарный неврит (нейросенсорная тугоухость) — это воспалительный процесс в слуховом нерве, который характеризуется угнетением слуха, возникновением болевых ощущений, шумом в ушах, потерей равновесия. Причины патологии могут быть врождёнными или приобретёнными. Опасность болезни в том, что симптомы могут развиваться медленно, но возможно потерять слух внезапно, в течение нескольких часов. Для диагностики и лечения нужно обращаться к оториноларингологу и неврологу.
Причины кохлеарного неврита слухового нерва
Происхождение патологии может быть как на генетическом уровне, так и полученным вследствие различных факторов:
Статью проверил
Дата публикации: 24 Марта 2021 года
Дата проверки: 24 Марта 2021 года
Дата обновления: 01 Декабря 2021 года
Содержание статьи
Симптомы
Характерные признаки патологии проявляются внезапно, но бывают случаи, когда симптоматика не проявляется до возникновения серьёзных нарушений. На первом этапе у больного наблюдают незначительное снижение слуха, как правило, на одну сторону. Дальнейшее развитие неврита зависит от того, как быстро пациент обратился к врачу и какие причины спровоцировали недуг. Самые распространнёные симптомы кохлеарного неврита:
Разновидности
Кохлеарный неврит различают по форме, происхождению, этапам развития:
Острую стадию можно вылечить окончательно, если сразу предпринять меры и начать лечение. Подострая форма чаще переходит в хроническую. Прогрессирующий этап считается самым опасным — именно в этот период повышается риск получить глухоту.
Диагностика
Диагностические исследования назначают в комплексе — обычно это осмотр больного, неврологические и акустические тесты, а также инструментальные методики:
Особенности комплексной терапии периферических кохлеовестибулярных расстройств
Приведены результаты клинического наблюдения, наглядно подтверждающего эффективность совместного использования препаратов бетагистина дигидрохлорид и пирацетам в терапии периферических кохлеовестибулярных нарушений. Лечение позволило добиться стойкого кл
There are some results of clinical observation that credibly confirm the efficiency of combined use of medications betahistine dihydrochloride and Piracetam in the therapy of peripheral cochlear-vestibular disorders. The treatment allowed to achieve sustainable clinical effect.
Изучение проблемы эффективности терапии периферических кохлеовестибулярных нарушений (ПКВН) дает возможность констатировать, что определяющее значение в ее решении принадлежит тщательному обследованию пациента в соответствии с современными возможностями и своевременному, этиопатогентически обоснованному индивидуализированному комплексу лечебно-реабилитационых мероприятий. Важным в практическом отношении следует считать грамотную трактовку результатов диагностического обследования пациента, анализ отличительных особенностей конкретного клинического случая и выработку оптимальной схемы фармакотерапии в сочетании с немедикаментозными лечебными мероприятиями. Перечень лекарственных препаратов, используемых при ПКВН, достаточно широк, среди них бетагистина дигидрохлорид и пирацетам — одни из наиболее часто назначаемых больным со слуховыми и вестибулярными расстройствами как на этапе лечения, так и на этапе медицинской реабилитации пациентов.
Цель данной публикации — демонстрация клинического наблюдения, наглядно подтверждающего эффективность совместного использования препаратов бетагистина дигидрохлорид (Бетасерк) 24 мг 2 раза в сутки и пирацетам 1200 мг 2 раза в сутки в течение двух месяцев при ПКВН.
Мужчина 50 лет наблюдается врачом-оториноларингологом в течение трех лет по поводу правостороннего периферического кохлеовестибулярного синдрома. Жалобы на снижение слуха на правое ухо, низкочастотный постоянный шум в правом ухе, периодическую неустойчивость при ходьбе.
В анамнезе: шесть лет назад была диагностирована гипертоническая болезнь, постоянно принимает гипотензивные препараты, однако при волнении и переутомлении возникают эпизоды артериальной гипертензии до 160/100 мм рт. ст. В течение многих лет курит (около одной пачки сигарет в день), алкоголь употребляет умеренно. Начало заболевания связывает с перенесенным «на ногах» гриппом. Три года назад обратился к оториноларингологу-отоневрологу спустя двое суток от начала заболевания с жалобами на резкое вращательное головокружение, снижение слуха на правое ухо, резкий высокочастотный шум в нем. На первичном приеме была диагностирована «острая правосторонняя сенсоневральная тугоухость с явлениями вестибулярной дезадаптации за счет периферической вестибулярной правосторонней гиперрефлексии». В связи с установленным диагнозом проведено лечение в стационаре (пентоксифиллин, пирацетам, витамины группы В парентерально, бетагистина дигидрохлорид, курс классической акупунктуры) с улучшением.
При обследовании: при осмотре констатирована нормальная отоскопическая картина, шепотная речь слева — 6 м, справа — 3 м. Результаты камертональных проб: W→, +R+. По данным тональной пороговой аудиометрии: правосторонняя сенсоневральная тугоухость (повышение порогов до 10–20 дБ по воздушной и костной проводимости на частотах 1000–8000 Гц, без отрицательной динамики в течение всего периода амбулаторного наблюдения. Спонтанный нистагм отсутствует, координация и статика не нарушены, в том числе по данным стабилометрического исследования. Калорическая проба выявляет гипорефлексию нистагма по длительности и амплитуде с акцентом от правого лабиринта.
При дополнительном обследовании: МРТ головного мозга с контрастным усилением: картина хронической ишемии головного мозга, МР-данных за патологический процесс в проекции мостомозжечковых углов не получено. МРТ шейного отдела позвоночника: протрузии межпозвонковых дисков С3-С7, спондилоартроз.
Дуплексное сканирование брахиоцефальных сосудов — атеросклеротические изменения экстракраниальных отделов брахиоцефальных артерий, гемодинамически значимый S-образный изгиб правой позвоночной артерии.
Диагноз: правосторонний хронический периферический кохлеовестибулярный синдром.
Лечение: при первичном обращении в связи с установленным диагнозом (острый правосторонний периферический кохлеовестибулярный синдром) проведено лечение в оториноларингологическом стационаре: пентоксифиллин внутривенно капельно № 10, витамины группы В парентерально, мочегонные препараты, курс классической акупунктуры, массаж шейногрудного отдела позвоночника, курс гидроаэроионизации. Пирацетам применяли внутримышечно по 5 мл 2 раза в день в течение 10 суток, далее — внутрь по 1200 мг 2 раза в сутки. Бетагистина дигидрохлорид (Бетасерк) 24 мг 2 раза в сутки назначали по окончании курса парентеральной терапии. После выписки из стационара пациент до двух месяцев продолжил прием пирацетама 1200 мг 2 раза в сутки и Бетасерка 24 мг 2 раза в сутки, проведен второй курс рефлексотерапии. В последующем на протяжении всего периода наблюдения дважды в год, в весенний и осенний периоды, пациенту проводится поддерживающая фармакотерапия, включающая совместный прием бетагистина дигидрохлорида 24 мг 2 раза в сутки и пирацетама 1200 мг 2 раза в сутки в течение двух месяцев. На фоне лечения пациент отмечает уменьшение шума в правом ухе, большую устойчивость при ходьбе. Переносимость проводимой терапии хорошая — побочных явлений, аллергических реакций зарегистрировано не было.
Обоснование лечебной тактики: рациональным в данном клиническом примере следует считать комбинацию фармакотерапии и немедикаментозных методов лечения: совместный прием бетагистина дигидрохлорида (Бетасерк) 24 мг 2 раза в сутки и пирацетама 1200 мг 2 раза в сутки в течение двух месяцев, а также курсы корпорально-аурикулярной акупунктуры (см. рис. «Алгоритм обследования пациентов с головокружением в амбулаторных условиях» на стр. 50) [2–5, 9]. Обоснованием совместного применения бетагистина гидрохлорида и пирацетама, с точки зрения практики врача, является этиопатогенетическая обоснованность, взаимодополняемость, отсутствие антагонистического взаимодействия и хорошая переносимость данного способа фармакотерапии. Основанием для применения бетагистина дигидрохлорида является избирательность его вазоактивного действия, улучшение микроциркуляции внутреннего уха и проницаемости капилляров, нормализация давления эндолимфы в лабиринте. Препарат положительно влияет на передачу нервного импульса в медиальных и латеральных вестибулярных ядрах и периферических вестибулярных рецепторных образованиях [2, 4]. Бетасерк не только оказывает вестибулолитический эффект, но и ускоряет компенсацию статокинетической функции [8]. Для пациента, страдающего гипертонической болезнью и постоянно принимающего гипотензивные препараты, принципиально важно, что прием бетагистина дигидрохлорида не влияет на уровень артериального давления. С практической точки зрения важно отметить, что основанием к назначению Бетасерка в составе комплексной терапии с пирацетамом данному пациенту служат также результаты дуплексного сканирования брахиоцефальных сосудов, указывающих на вертеброгенную составляющую в формировании кохлеовестибулярных нарушений.
Бетасерку свойственна хорошая переносимость, а также такое важное для длительного амбулаторного приема качество, как отсутствие седативного эффекта и неинвазивность [2, 4]. Периферические кохлеовестибулярные нарушения у данного пациента протекают на фоне хронической ишемии головного мозга, что лишний раз подтверждает существующее положение о взаимосвязи ангиогенной сенсоневральной тугоухости и сосудистых поражений головного мозга [1, 3]. Обосновано применение пирацетама как ноотропного средства, оказывающего непосредственное воздействие на центральную нервную систему, оптимизирующего метаболические процессы в нервных клетках, улучшающего синаптическую проводимость. Важное свойство препарата заключается в способности улучшать микроциркуляцию за счет нормализации реологических свойств крови без вазодилатационного эффекта. Пирацетам ингибирует агрегацию тромбоцитов, восстанавливает эластичность мембраны эритроцитов, снижает адгезию эритроцитов. Антигипоксантное и детоксикационное действие реализуется посредством протекторного и восстанавливающего воздействия на центральную нервную систему [2, 6].
Эффективность фармакотерапии периферических кохлеовестибулярных нарушений повышает включение в комплекс терапевтических и реабилитационных мероприятий рефлексотерапии, основанной на стимуляции рецепторных структур кожи дифференцированно, по биологически активным точкам с повышенной концентрацией рецепторных аппаратов различной модальности. Терапевтический эффект рефлексотерапии объясняется местным (сегментарным) и общим (генерализованным) действием. Местные реакции обусловлены изменением кровенаполнения, температуры, чувствительности, величины электрокожного сопротивления и потенциала в зоне воздействия, что является источником длительной импульсации в различные отделы нервной системы человека. Одновременно развивается генерализованная реакция как результат поступления афферентной импульсации по спино-ретикулярному, спино-таламическому путям в высшие отделы нервной системы, вызывающей изменения функционального состояния всех структур мозга с ответной обратной реакцией [5, 7].
Таким образом, добиться стойкого клинического эффекта в данном сложном, с точки зрения полиэтиологичности и коморбидности, случае позволило проведение комплексного лечения, включающего медикаментозную терапию (рациональное сочетание двух препаратов: бетагистина дигидрохрорид (Бетасерк) 24 мг 2 раза в сутки и пирацетам 1200 мг 2 раза в сутки в течение двух месяцев), дополненную курсовой корпорально-аурикулярной акупунктурой.
Статья подготовлена при поддержке компании Эбботт.
Литература
С. В. Морозова, доктор медицинских наук, профессор
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова Минздравсоцразвития России, Москва
Кохлеовестибулярные нарушения: подходы к диагностике и лечению
Опубликовано в журнале:
Вестник оториноларингологии, 5, 2011
Cochleovestibular disorders: approaches to diagnostics and treatment
O.V. ZAITSEVA
ФГУ НКЦ оториноларингологии ФМБА России (дир. — проф. Н.А. Дайхес), МОНИКИ им. М.Ф. Владимирского (дир. — член-корр. РАМН проф. Г.А. Оноприенко), Москва
Проведена оценка эффективности включения Мильгаммы и Мильгаммы композитум в схему лечения пациентов с кохлеовестибулярными нарушениями. В результате проведенного лечения у пациентов, получавших Мильгамму и Мильгамму композитум, вестибулярная компенсация (в том числе по данным постурографических показателей) достигалась в более короткие сроки — через 3—4 нед от начала лечения, тогда как у пациентов, не получавших эти препараты, — через 5 нед. Таким образом, можно рекомендовать применение Мильгаммы и Мильгаммы композитум в качестве нейротропных средств, дополняющих базовую терапию у пациентов с кохлеовестибулярными нарушениями для сокращения сроков достижения вестибулярной компенсации.
Ключевые слова: кохлеовестибулярные нарушения, головокружение, нарушения равновесия, сенсоневральная тугоухость, Мильгамма, Мильгамма композитум.
The aim of this work was to evaluate the efficacy of introduction of milgamma and milgamma compositum in the treatment of 52 patients with cochleovestibular disorders of different etiology. Thirteen patients enrolled in the study received standard therapy and 39 others were given its combination with milgamma preparations. Combined therapy with milgamma and milgamma compositum ensured faster vestibular compensation including posturographic characteristics than the standard treatment (within 3—4 weeks compared with 5 weeks in controls). The results of the study give reason to recommend milgamma and milgamma compositum as neurotropic medicines in addition to standard therapy for the management of the patients presenting with cochleovestibular disorders for the acceleration of the vestibular compensation.
Key words: cochleovestibular disorders, dizziness, balance disorder, sensorineural loss of hearing, milgamma, milgamma compositum.
Актуальность проблемы кохлеовестибулярных нарушений определяется в первую очередь высоким уровнем заболеваемости с преобладанием лиц наиболее активного и трудоспособного возраста [1—4]. Так, при опросе более 20 тыс. человек в возрасте от 18 до 64 лет выяснилось, что за последний месяц более 20% испытали головокружение, из них свыше 30% страдают головокружением на протяжении более 5 лет [5]. Около трети пациентов, обращающихся к оториноларингологам, высказывают жалобы на различные типы головокружения. В Российской Федерации число больных с кохлеовестибулярными нарушениями составляет 13—14 человек на 10 тыс. населения [6]. Следует отметить, что детальное вестибулометрическое исследование больных острой сенсоневральной тугоухостью в ряде случаев позволяет выявить нарушения функции лабиринта [2]. Установленная по результатам калорической и вращательной проб экспериментальная вестибулярная гипо- или гиперрефлексия, а также выявленная в ходе стабилометрического исследования статическая атаксия даже при отсутствии спонтанной вестибулярной симптоматики дает основания расценивать такое состояние больного, как кохлеовестибулярное нарушение [7]. Считается, что при сенсоневральной тугоухости наиболее часто регистрируется симптоматика, характерная для периферического вестибулярного синдрома угнетения [2].
Периферические вестибулярные расстройства возникают при поражении сенсорных элементов ампулярного аппарата и преддверия, вестибулярного ганглия и нервных проводников ствола мозга [8].
Периферическое вестибулярное головокружение — это чаще головокружение приступообразного характера различной интенсивности (от слабых до бурных атак), сопровождающееся спонтанным нистагмом — клоническим горизонтальным или горизонтально-ротаторным, разной интенсивности, степени, ассоциированным с гармоничным отклонением туловища и рук в сторону медленного компонента. Отмечается положительное влияние поворота головы (в сторону медленного компонента нистагма). Как правило, периферическое вестибулярное головокружение бывает односторонним и нередко сопровождается нарушением слуховой функции на пораженной стороне. Экспериментальные пробы выявляют угнетение функции вестибулярных рецепторов (кроме начального периода заболевания) [9].
Установление причины кохлеовестибулярного расстройства весьма важно, поскольку это обеспечивает возможность проведения патогенетически обоснованного лечения и выбора адекватной профилактической тактики.
Обследование пациентов с кохлеовестибулярными нарушениями должно быть детальным и всесторонним и обязательно включать обследование у отоневролога, позволяющее оценить функциональное состояние вестибулярного анализатора и уровень его поражения.
Расстройство функции равновесия (атаксия), являясь неотъемлемой частью кохлеовестибулярных нарушений, существенно ухудшает качество жизни: пациенты нередко оказываются неспособными без посторонней помощи передвигаться даже в пределах собственного жилища. Поэтому при оценке состояния вестибулярной функции большое внимание уделяется исследованию способности человека поддерживать вертикальное положение тела — функции равновесия, осуществляющейся посредством установочных рефлексов, которые удерживают центр массы тела в пределах проекции площади его опоры.
Одним из способов выявления атаксии является цифровая постурография. Применявшиеся ранее методики проведения стабилографического исследования предполагали проведение проб, часто мучительных для пациента: обследование на аппарате, конструкция которого предусматривала качательные движения в горизонтальной и сагиттальной плоскостях, которые регистрировались на ЭВМ, контроль спонтанных и поствращательных отклонений при помощи «пишущего стержня» и шкалы, прикрепленных к креслу Барани [10]. Позднее для выявления нарушений статокинетической устойчивости были предложены пробы, не сопровождающиеся вегетосенсорными проявлениями: медленные наклоны головы в сагиттальной и фронтальной плоскости, повороты головы вправо и влево с последующей ходьбой по прямой линии, а также алгоритм «пятка—носок», шагательная проба [11].
Использование современной аппаратуры значительно расширило диагностические возможности проведения статокинетических исследований, позволило проводить информативную качественную и количественную оценку функции равновесия. Современным вариантом позы Ромберга является проведение исследования на стабилометрической платформе, являющейся центром прибора, оценивающего функцию равновесия в количественном отношении [12]. Для дифференциальной диагностики различных нарушений функции равновесия используются нагрузочные функциональные пробы с одновременной постурографией: пробы с оптокинетической стимуляцией, с максимальным поворотом головы вправо и влево, с дозированной пороговой вращательной стимуляцией, с фиксацией взора [13].
Лечение пациентов с кохлеовестибулярными нарушениями должно быть незамедлительным и этиотропным и включать наряду с вестибулярной реабилитацией использование вазоактивных, антихолинергических, нейротропных препаратов (высокие дозы витаминов группы В) [6, 14]. Витамины группы B, прежде всего В1, В6 и В12, многие годы применяются в комплексном лечении заболеваний периферической нервной системы с целью улучшения обменных и усиления регенеративных процессов в нейроэпителии и замедления развития нейропатии [15].
Витамин В1 (тиамин) участвует в энергетических процессах в нервных клетках, в частности в цикле Кребса [16], и регенерации поврежденных нервных волокон [6, 17—19].
Витамин В6 (пиридоксин) является кофактором более чем для 100 ферментов, а благодаря способности регулировать метаболизм аминокислот нормализует белковый обмен [20, 21]. Кроме того, в последние годы доказано, что витамин В6 имеет антиоксидантное действие [22], участвует в синтезе катехоламинов, гистамина и гаммааминомасляной кислоты, увеличивает внутриклеточные запасы магния, также играющего важную роль в обменных процессах нервной системы.
Витамин В12 (цианокобаламин) играет важную роль в делении клеток, кроветворении, регуляции обмена липидов и аминокислот. Он участвует в важнейших биохимических процессах миелинизации нервных волокон [23].
В настоящее время оториноларингологи редко используют водорастворимые препараты витаминов В1, В6 и В12 для монотерапии, так как наиболее эффективным считается их комплексное применение [24]. Одним из наиболее эффективных современных инъекционных В-комплексов считается препарат Мильгамма («WÖRWAG PHARMA GmbH & Co. KG», Германия). Мильгамма представляет собой комбинацию синергично действующих нейротропных витаминов В1, В6 и В12. Каждая ампула препарата содержит по 100 мг тиамина гидрохлорида и пиридоксина гидрохлорида, 1000 мг цианокобаламина. Входящий в состав Мильгаммы местный анестетик лидокаин (20 мг) позволяет сделать инъекции практически безболезненными. Следует отметить, что Мильгамма имеет небольшой объем ампулы — всего 2 мл. Это повышает приверженность пациента терапии. Последовательное назначение Мильгаммы и Мильгаммы композитум при различных заболеваниях нервной системы способствует восстановлению функции нервных тканей при невропатиях различного происхождения [25, 26]. В частности, эффективность применения Мильгаммы при сенсоневральной тугоухости подтверждена проведенными в последние годы исследованиями [15, 27].
В период с января 2008 г. по май 2011 г. проведено консервативное лечение 52 пациентов в возрасте от 18 до 43 лет (23 женщины и 29 мужчин) с кохлеовестибулярными нарушениями. Причиной кохлеовестибулярных нарушений у 21 пациента явилась перенесенная острая респираторная вирусная инфекция, у 19 — стрессовый фактор, у 12 — подъем артериального давления. Всем пациентам проводилось комплексное аудиологическое и вестибулологическое исследование, включавшее исследование спонтанной отоневрологической симптоматики, оптокинетического нистагма (скорость движения стимула 15°/с, 30°/с и 45°/с), тесты плавного зрительного слежения, зрительных саккад, позиционный тест Дикса—Холлпайка, битермальный бинауральный калорический тест, вращательный тест с записью движения глаз на видеоокулографическом комплексе VNG Stad Alone Unit VO 25 («Heinemann Medizintechnik GmbH», Германия), исследование статики, координации на постурографическом комплексе Smart EquiTest Balans Master («NeuroCom», США), электрокохлеография на установке Viking Ques («Nicolet», США) и/или дегидратационный тест с ксилитом.
Повторная аудиометрия и вестибулометрия проводились сразу по окончании лечения и спустя 2 мес, цифровая постурография выполнялась еженедельно на протяжении курса лечения и также спустя 2 мес. Выраженность головокружения оценивали по критериям выраженности функциональных нарушений Международной классификации функций ВОЗ: 0 — нет (никаких, ничтожные), 1 — легкие (незначительные, слабые), 2 — умеренные (средние, значимые), 3 — тяжелые (высокие, интенсивные), 4 — абсолютные (полные) [29].
Дополнительные исследования включали: рентгенографию височных костей по Стенверсу, при необходимости магнитно-резонансную томографию головного мозга/внутренних слуховых проходов и мостомозжечковых углов; рентгенографию шейного отдела позвоночника, экстра- и транскраниальную допплерографию. Всем больным выполняли общеклинические анализы крови и мочи, биохимический анализ крови, коагулограмму.
Спонтанная вестибулярная симптоматика в виде координаторных нарушений зарегистрирована у 34 (65%) человек. Спонтанный нистагм выявлен у 12 (23%) пациентов — нистагм был горизонтальный, мелкоразмашистый, клонический, I степени. Вестибулярная гипо- или гиперрефлексия (по результатам калорической и вращательной проб) зарегистрирована у всех пациентов. Гипорефлексия проявлялась отсутствием или продолжительностью калорического нистагма не более 40 с. Продолжительность нистагма в среднем составила 18±4 с. При гиперрефлексии продолжительность калорического нистагма увеличивалась до 80—100 с и составила в среднем 91±6 с (без диссоциации). Выраженность головокружения на момент начала лечения пациенты оценивали в среднем на 2,8±0,5 балла по критериям выраженности функциональных нарушений Международной классификации функций ВОЗ.
При аудиологическом исследовании нарушение звуковосприятия зарегистрировано у всех пациентов, в том числе двустороннее — у 38. Эндолимфатический гидропс при проведении электрокохлеографии и/или дегидратационного теста (с ксилитом) ни у одного из пациентов не выявлен.
При проведении цифровой постурографии (тест чувствительной организации — Sensory organization test (SOT)) у всех пациентов зарегистрирована статическая атаксия за счет вестибулярной составляющей. SOT — современный вариант теста Ромберга, выполняемый в 6 этапов: с открытыми и закрытыми глазами на неподвижной платформе при неподвижном окружении, с открытыми глазами на неподвижной платформе при подвижном окружении, с открытыми и закрытыми глазами на подвижной платформе при неподвижном окружении и с открытыми глазами на подвижной платформе при подвижном окружении. Базовое лечение пациентам проводилось в соответствии со сложившимися стандартами оказания медицинской помощи (с учетом противопоказаний) и включало применение пентоксифиллина, пирацетама, винпоцетина, бетагистина в течение 6 нед. В течение 4—6 нед всем пациентам проводилась вестибулярная реабилитация на постурографическом комплексе Smart EquiTest Balans Master («NeuroCom», США) 3—5 раз в неделю по индивидуальной программе. 12 человек продолжали прием гипотензивных препаратов центрального действия и диуретиков, назначенных ранее кардиологом или терапевтом. 19 пациентов с кохлеовестибулярными нарушениями постстрессовой этиологии по рекомендации невролога получали антидепрессант растительного происхождения. Пациенты, перенесшие острую респираторную вирусную инфекцию (21 человек), в течение первых 3 дней получали парентеральную дезинтоксикационную терапию (реополиглюкин или раствор глюкозы 5%, аскорбиновая кислота 5%).
39 человек (19 женщин и 20 мужчин в возрасте от 18 до 43 лет) получали помимо базовой терапии препараты Мильгамма и Мильгамма композитум по схеме: Мильгамма внутримышечно №10, затем по 1 драже Мильгаммы композитум 3 раза в день в течение 6 нед.
13 пациентам (6 женщинам и 7 мужчинам в возрасте от 20 до 43 лет) Мильгамма и Мильгамма композитум не назначались в связи с индивидуальной непереносимостью витаминов В-группы; они получали только препараты базовой терапии.
Данные отоневрологического и аудиологического исследований у пациентов, получавших и не получавших препараты Мильгамма и Мильгамма композитум, были сравнимы.
Данные компьютерной постурографии с автоматическим расчетом показателей, в частности индекса вестибулярной устойчивости, измеряемого в процентах, — отношение суммарной амплитуды смещения центра тяжести к абсолютному центру платформы — у пациентов обеих групп, получавших препараты Мильгамма и Мильгамма композитум, были также сравнимы и достоверно (р
В результате проведенного лечения у всех пациентов при проведении контрольной постурографии на момент окончания курса зафиксировано уменьшение статической атаксии, что выразилось в достоверном (рОднако у пациентов, принимавших Мильгамму и Мильгамму композитум, нормализация постурографических показателей наступала в среднем на 2 нед раньше и индекс вестибулярной устойчивости по окончании лечения был достоверно (р
| Сроки обследования в процессе лечения | Базовое лечение (n=13) | Базовое лечение+Мильгамма и Мильгамма композитум (n=39) |
| До начала лечения | 49±7 | 47±10 |
| От начала лечения | ||
| через 1 нед | 53±8 | 60±7 |
| через 2 нед | 59±4 | 67±6 |
| через 3 нед | 64±5 | 72±6 |
| через 4 нед | 70±6 | 79±4 |
| через 5 нед | 72±3 | 83±6 |
| через 6 нед | 78±6 | 85±7 |
| Спустя 2 мес после лечения | 81±5 | 86±6 |
Как видно из таблицы, у пациентов, получавших Мильгамму и Мильгамму композитум, стойкая нормализация основного постурографического показателя — индекса вестибулярной устойчивости (норма ≥70), достигалась в более короткие сроки — через 3—4 нед от начала лечения, тогда как у пациентов, получавших только базовую терапию, — через 5 нед.
Выраженность головокружения на момент окончания лечения пациенты в среднем оценивали на 0,3±0,2 балла по критериям выраженности функциональных нарушений Международной классификации функций ВОЗ (достоверной разницы в оценке выраженности головокружения среди пациентов обеих групп не было). У всех пациентов к окончанию курса лечения зафиксирована компенсация вестибулярной функции в покое, сочетавшаяся с положительной динамикой показателей повторной вестибулометрии. Повторное аудиологическое исследование показало, что у получавших Мильгамму и Мильгамму композитум пациентов слух улучшился в среднем на 24±0,8 дБ, что достоверно (р
Нежелательных явлений (т.е. любых неблагоприятных медицинских явлений, наблюдаемых у использующего медицинский продукт пациента, которое может и не иметь причинно-следственной связи с данным видом лечения) ни у кого из пациентов, в том числе получавших сопутствующую терапию, зафиксировано не было, лечение все переносили хорошо. Со слов пациентов, ни у одного из них за весь период наблюдений эпизодов вращательного головокружения не возникало. Таким образом, можно рекомендовать применение Мильгаммы и Мильгаммы композитум в качестве нейротропных средств, дополняющих базовую терапию у пациентов с кохлеовестибулярными нарушениями для сокращения сроков достижения вестибулярной компенсации и улучшения слуховой функции.