Вагинальная атрофия: этиологические аспекты и современные подходы к терапии
Согласно прогнозам, к 2030 г. в мире число женщин в постменопаузе достигнет 1,2 млрд. Эстрогендефицитное состояние в период климактерия у 15–57% женщин приводит к развитию вагинальной атрофии. В обзоре приводятся последние данные, касающиеся вопросов пато
Постменопауза характеризуется эстрогендефицитным состоянием у женщин, обусловленным возрастным снижением, а затем и прекращением функции яичников [1]. Как известно, любые эпителиальные ткани реагируют на изменение окружающей их гормональной среды сходным образом, но ни одна из них не может сравниться с эпителием свода влагалища и шейки матки по скорости и отчетливости реакции на гормоны, в первую очередь на половые стероиды [2]. Таким образом, урогенитальный тракт особенно чувствителен к снижению уровня эстрогенов и около половины всех женщин в постменопаузе испытывают симптомы, связанные с урогенитальной атрофией (УГА), затрагивающие половую функцию и качество жизни [3]. В клинической картине урогенитальных расстройств в климактерическом периоде выделяют симптомы, связанные с атрофией влагалища (вагинальная атрофия (ВА)), и расстройства мочеиспускания (цистоуретральная атрофия). В отличие от вазомоторных симптомов, которые обычно проходят со временем, симптомы вагинальной атрофии, как правило, возникают в пременопаузе и прогрессируют в постменопаузальном периоде, приводя к функциональным и анатомическим изменениям [4]. У 15% женщин в пременопаузе и 40–57% женщин в постменопаузе отмечаются симптомы ВА [5], такие как сухость влагалища 27–55%, жжение и зуд 18%, диспареуния 33–41%, а также повышенная восприимчивость к инфекционным заболеваниям органов малого таза 6–8% [4], что значительно ухудшает состояние здоровья, негативно влияет на общее и сексуальное качество жизни [6]. У 41% женщин в возрасте 50–79 лет есть хотя бы один из симптомов ВА [10].
Стенки влагалища состоят из трех слоев: внутреннего слоя, который выстлан многослойным плоским эпителием; среднего мышечного и наружного соединительнотканного слоев (или волокнистого слоя). Атрофические процессы, захватывающие соединительнотканные и мышечные структуры влагалища, а также мышцы тазового дна, уретры, мочевого пузыря, особенно выражены в слизистой влагалища. Известно, что у женщин слизистая оболочка влагалища состоит из четырех основных слоев эпителиальных клеток: базальный слой; парабазальный слой (или митотически-активный); промежуточный гликогенсодержащий слой; поверхностный (слущивающийся) [11]. Эстрогеновые рецепторы располагаются в основном в базальном и парабазальном слоях влагалища и практически отсутствуют в промежуточном и поверхностном [10]. Дефицит эстрогенов блокирует митотическую активность базального и парабазального слоев эпителия влагалищной стенки, а следовательно, и пролиферацию влагалищного эпителия [12]. Следствием прекращения пролиферативных процессов во влагалищном эпителии является исчезновение гликогена — питательной среды для лактобактерий, таким образом из влагалищного биотопа полностью элиминируется его основной компонент — лактобациллы [3, 12].
Известно, что перекись-продуцирующие лактобациллы, преобладающие в микробиоцинозе влагалища у женщин репродуктивного возраста, играют ключевую роль в предотвращении появления заболеваний урогенитального тракта [10, 11]. Вследствие расщепления гликогена, который образуется в эпителии влагалища при условии наличия достаточного количества эстрогенов, образуется молочная кислота, обеспечивающая кислую среду влагалища (в пределах колебаний рН от 3,8 до 4,4). Подобный защитный механизм приводит к подавлению роста патогенных и условно-патогенных бактерий. В период постменопаузы слизистая оболочка влагалища утрачивает эти защитные свойства, истончается, легко травмируется с последующим инфицированием не только патогенными, но и условно-патогенными микроорганизмами.
Эстрогены являются главными регуляторами физиологических процессов во влагалище. Эстрогеновые рецепторы α присутствует во влагалище в пременопаузе и постменопаузе, в то время как эстрогеновые рецепторы β полностью отсутствуют или имеют низкую экспрессию в вагинальной стенке у женщин в постменопаузе. Наиболее высокая плотность эстрогеновых рецепторов наблюдается во влагалище и уменьшается по направлению от внутренних половых органов к коже. Плотность андрогеновых рецепторов, наоборот, низкая во влагалище и более высокая в области наружных половых органов. Рецепторы прогестерона встречаются только во влагалище и эпителии вульвовагинального перехода [10]. Поскольку в клетках стромы влагалища содержатся рецепторы к эстрогенам, то коллаген, входящий в состав соединительной ткани влагалищной стенки, является эстроген-чувствительной структурой, содержание которого уменьшается по мере прогрессирования эстрогенного дефицита. Так как рецепторы к эстрогенам располагаются не только в эпителии и строме влагалищной стенки, но и в эндотелии сосудов, в постменопаузе отмечается снижение кровообращения во влагалище до уровня различной степени ишемии. К тому же эстрогены являются вазоактивными гормонами, которые увеличивают приток крови, стимулируя высвобождение эндотелиальных медиаторов, таких как оксид азота, простагландины и фактор гиперполяризации эндотелия. Подобное прогрессирующее снижение кровотока в слизистой влагалища приводит к гиалинизации коллагеновых и фрагментации эластических волокон, увеличивая количество соединительной ткани [12].
Эстрогеновые рецепторы были также обнаружены на вегетативных и сенсорных нейронах во влагалище и вульве. В исследовании T. L. Griebling, Z. Liao, P. G. Smith было выявлено уменьшение плотности сенсорных ноцицептивных нейронов во влагалище на фоне лечения эстрогенами. Эта особенность может быть полезна в целях устранения дискомфорта, связанного с ВА, а именно в облегчении симптомов, таких как жжение, зуд и диспареуния, с которыми сталкиваются многие женщины в постменопаузе [5, 10].
Атрофия слизистой вульвы и влагалища характеризуется истончением эпителия, уменьшением вагинальной складчатости, побледнением, наличием петехиальных кровоизлияний, признаков воспаления. Также вследствие инволютивных изменений происходит потеря упругости тканей, подкожно-жировой клетчатки и выпадение лобковых волос, снижение секреторной активности бартолиниевых желез [3, 13, 14]. Как правило, врачи диагностируют атрофию вульвы и влагалища на основании сочетания клинических симптомов и визуального осмотра. Исследователи все чаще настаивают на более объективных и воспроизводимых способах диагностики, не исключая субъективные жалобы пациента [13]. Исторически сложилось, что для диагностики ВА необходимы два основных объективных способа диагностики и оценки эффективности лечения: рН влагалища, а также подсчет вагинального индекса созревания (ВИС, преобладание клеток базального и парабазального слоев) [12, 13]. Интересно, что степень атрофических изменений, измеряемая индексом созревания, не всегда коррелирует с симптомами [15]. В исследовании, проведенном среди 135 менопаузальных женщин-добровольцев, которые прошли оценку симптомов, а затем рейтинг «вагинального здоровья» (оценка цвета влагалища, выделений, целостности и толщины эпителия, рН) и измерение индекса созревания, исследователи обнаружили слабую корреляцию между физическими проявлениями и индексом созревания.
Гормональные изменения, происходящие в течение жизненного цикла, оказывают влияние на вагинальную флору начиная от момента рождения до периода постменопаузы. Снижение эстрогенов в перименопаузе и постменопаузе приводит к уменьшению количества лактобактерий и изменению флоры в целом. Согласно данным S. L. Hillier, R. J. Lau, при детальном анализе микрофлоры влагалища 73 женщин в постменопаузе, не принимавших гормональную терапию, в 49% случаев не было выявлено лактобацилл. А среди тех, у которых они обнаруживались, концентрация последних была в 10–100 раз меньше, чем у женщин в пременопаузе [15]. В постменопаузе наиболее распространенными микроорганизмами являлись анаэробные грамотрицательные палочки и грамположительные кокки.
Несмотря на вышесказанное, у некоторых женщин симптомы атрофии прогрессируют вскоре после наступления менопаузы, а у других они не возникают даже в более поздние годы. Среди факторов, которые могут увеличить риск развития урогенитальной атрофии, курение является одним из наиболее изученных. Курение оказывает прямое воздействие на плоскоклеточный эпителий влагалища, снижает биодоступность эстрогена и уменьшает перфузию крови. Другими гормональными факторами, которые, как правило, имеют значение, являются уровни различных андрогенов, таких как тестостерон и андростендион. Предполагают, что после менопаузы у женщин с более высоким уровнем андрогенов, которые поддерживают сексуальную активность, отмечено меньше изменений, связанных с атрофией [12]. Кроме того, ВА наблюдается чаще у женщин, которые никогда не рожали через естественные половые пути [16].
Принимая во внимание патогенез заболевания, терапия эстрогенами является золотым стандартом лечения. Все клинические рекомендации по лечению УГА сходятся во мнении, что наиболее распространенным и эффективным методом лечения является системная или локальная гормональная терапия эстрогенами в различных формах, так как она достаточно быстро улучшает индекс созревания и толщину слизистой оболочки влагалища, снижает рН влагалища и устраняет симптомы ВА [3, 11–13]. Для лечения УГА, сочетающейся с симптомами климактерия, используют системную гормональную терапию. В остальных случаях отдают предпочтение местному лечению, которое позволяет избежать большинства системных побочных эффектов [12, 13]. Исследования показали, что системная заместительная гормональная терапия устраняет симптомы ВА в 75% случаев, в то время как локальная терапия — в 80–90%.
Эстрогенсодержащие препараты для локального применения, представленные в форме крема, таблеток, пессариев/суппозиториев, вагинального кольца, могут содержать эстриол, конъюгированные эквинэстрогены, эстрадиол или эстрон. Из трех природных эстрогенов человеческого организма эстриол имеет самый короткий период полувыведения и наименьшую биологическую активность. В России имеется многолетний опыт локального применения эстриолсодержащих препаратов, обладающих выраженным кольпотропным эффектом. Учитывая слабое пролиферативное действие на эндометрий при использовании эстриола, дополнительное введение прогестагена не требуется. Многочисленные исследования показали, что ежедневное применение эстриола в дозе 0,5 мг оказывает заметный пролиферативный эффект на эпителий влагалища. Локальное применение эстриолсодержащих препаратов является безопасным и эффективным подходом к предотвращению и лечению ВА, не имеющим ограничений по возрастному аспекту и длительности лечения. В настоящее время в европейских странах отмечается тенденция к локальному использованию низких доз для эстрогенов эстриола и эстрадиола.
В 2006 г. в Кокрановском систематическом обзоре были проанализированы 19 клинических испытаний, в которых приняли участие 4162 женщины в постменопаузе, распределенные по группам, в зависимости от принимаемого вагинально препарата с эстрогенами, а конечной точкой в исследовании была оценка эффективности, безопасности и приемлемости терапии. Четырнадцать исследований сравнивали безопасность различных препаратов, семь акцентировали внимание на побочных эффектах и четыре на безопасности лечения и воздействии на эндометрий. Семь исследований включали плацебо-группы, и во всех показано улучшение состояния пациентов, принимающих гормональную терапию (табл.).
Результаты анализа показывают, что вагинальные таблетки с эстрадиолом более эффективны по сравнению с вагинальным кольцом и что оба варианта лечения превосходят плацебо в устранении диспареунии, сухости и зуда во влагалище. Вагинальный крем с конъюгированными лошадиными эстрогенами (КЛЭ) превосходит увлажняющие кремы в устранении сухости, повышении эластичности и объема кровотока во влагалище. Однако не было обнаружено никаких различий между тремя проанализированными препаратами терапии (крем с КЛЭ, таблетки с эстрадиолом и эстрадиол-рилизинг-кольцо) по отношению к количеству парабазальных клеток, кариопикнотическому индексу, индексу созревания и вагинальному индексу здоровья. К тому же также сообщаются данные об отсутствии значительных различий в толщине эндометрия, гиперплазии и количестве побочных эффектов между вагинальным кольцом, кремом или таблетками. Тем не менее, незначительный риск вагинальных кровотечений был описан во всех исследованиях, в которых применялись различные методы местной терапии эстрогенами, а также возможное увеличение риска развития кандидоза [16].
В результате метаанализа, проведенного Cardozo и соавт., показано, что вагинальный путь введения эстрогенов является эффективным методом лечения ВА. Комбинация местной и системной терапии позволяет достичь результатов в более сжатые сроки. Кроме того, низкие дозы местных эстрогенов: эстрадиола или эстриола так же эффективны, как и при системном введении. Было показано, что трансдермальный пластырь с ежедневной дозой в 14 мкг эстрадиола обладает аналогичным воздействием на рН влагалища и на индекс созревания, как и вагинальное кольцо с 7,5 мкг эстрадиола [17].
Положительный терапевтический эффект местной гормональной терапии был также отмечен в ситуациях, выходящих за рамки лечения ВА, а именно таких, как снижение риска рецидивирующих инфекций мочевыводящих путей и развития гиперактивного мочевого пузыря. С учетом вышеизложенного, эстрадиол-рилизинг-кольцо было одобрено в качестве лечения дизурии и ургентного недержания мочи. В то время как системная гормональная терапия, наоборот, увеличивает процент возникновения стрессового недержания мочи и почечных камней [10].
Таким образом, местная терапия имеет ряд преимуществ по сравнения с системным введением препаратов. Она позволяет избежать первичный метаболизм в печени, минимально воздействует на эндометрий, имеет низкую гормональную нагрузку, минимальные побочные эффекты, не требует добавления прогестагенов, оказывает в основном локальный эффект.
С практической точки зрения и в связи с аналогичной эффективностью и безопасностью всех местных препаратов с эстрогенами, пациентка должна иметь возможность выбрать препарат, который она считает наиболее подходящим для нее. Она должна быть проинформирована о том, что эффект достигается после одного-трех месяцев лечения. Дополнительное назначение прогестагенов не является обязательным при использовании локальных форм эстрогенов [18]. В обзоре за 2009 г., посвященном местной гормональной терапии, говорится, что ни в одном исследовании не наблюдали пролиферацию эндометрия после 6–24 месяцев использования эстрогенов, так что литература, таким образом, дает уверенность относительно безопасности малых доз вагинальных препаратов с эстрогенами и не поддерживает одновременное применение системных прогестагенов для защиты эндометрия [13].
Помимо перечисленных выше методов лечения ВА на сегодняшний момент существуют такие, как терапия с использованием дегидроэпиандростерона, селективных тканевых эстрогеновых комплексов, селективных модуляторов эстрогеновых рецепторов и негормональные методы лечения, а также комбинированные препараты, содержащие ультранизкодозированный эстриол и лактобактерии.
В работе U. Jaisamrarn и соавт. впервые оценивалась эффективность и переносимость ультранизких доз эстриола (0,03 мг) в сочетании с жизнеспособными Lactobacillus acidophilus в краткосрочной и долгосрочной перспективе лечения симптомов ВА. Было выявлено, что комбинация эстриола и лактобактерий в течение 12 недель была достаточна для достижения статистически и клинически значимых результатов, включающих улучшение объективных параметров (ВИС, рН, доля латобактерий в микрофлоре влагалища), а также качество жизни женщин [19].
Среди селективных модуляторов эстрогеновых рецепторов (SERM) оспемифен является наиболее современным лекарственным средством. В 12-недельном трехфазном рандомизированном исследовании с участием 826 женщин в постменопаузе изучали эффективность данного препарата в дозе 30 мг, 60 мг по сравнению с плацебо. К 4-й и 12-й неделям оспемифен в указанных ранее дозах показал статистически значимое увеличение количества поверхностных клеток, снижение парабазальных клеток и рН во влагалище по сравнению с плацебо. Сухость влагалища значительно снизилась как в группах с 30 мг и 60 мг по сравнению с плацебо к 12-й неделе, в то время как диспареуния уменьшилась только в группе, получавшей препарат в дозе 60 мг. В ходе исследования было выявлено, что побочный эффект препарата, проявляющийся в виде приливов, наблюдался у 9,6%, 8,3% и 3,4% участников в группах, получавших оспемифен в дозе 30 мг, 60 мг и плацебо соответственно. Толщина эндометрия от исходного уровня к 12-й неделе в среднем изменилась на 0,42 мм, 0,72 мм и 0,02 мм у участниц выше представленных групп соответственно [21].
Комбинация конъюгированных эстрогенов и базедоксифена — селективного модулятора эстрогеновых рецепторов, известная как тканевой селективный эстрогенный комплекс (TSEC), изучалась в исследовании 3-й фазы, где 601 женщина была распределена по группам в зависимости от ежедневной получаемой терапии: 20 мг базедоксифена плюс конъюгированные эстрогены 0,45 мг (BZA/CE), или базедоксифен 20 мг плюс 0,625 мг конъюгированные эстрогены, или 20 мг базедоксифена и плацебо. В ходе исследования было выявлено увеличение доли поверхностных клеток и уменьшение доли парабазальных от исходного уровня к 12-й неделе в большей степени в группе BZA/CE по сравнению с плацебо и только BZA. РН влагалища существенно не изменился по сравнению с исходным к окончанию исследования в группе BZA или плацебо, но значительно уменьшились в обеих группах BZA/CE. Тем не менее, снижение рН влагалища было значимо ниже в группе BZA/CE 20 мг/0,625 мг, чем в плацебо-группе. Самые «назойливые» симптомы значительно уменьшились к 12-й неделе по сравнению с плацебо в группе BZA/СЕ 20 мг/0,625 мг, но не в группе BZA/СЕ 20 мг/0,45 мг. Не отмечено каких-либо существенных различий в побочных эффектах или случаях прекращения участия в исследовании между группами. Однако была отмечена более высокая заболеваемость вагинитами в группах лечения (BZA/CE) по сравнению с плацебо [22]. Таким образом TSEC, а именно базедоксифен в сочетании с конъюгированными эстрогенами представляет собой альтернативу терапии прогестинами для защиты эндометрия от стимуляции эстрогенами, при сохранении благоприятного воздействия эстрогенов на симптомы, связанные с менопаузой.
Несмотря на перечисленные методы лечения ВА, не стоит забывать о профилактике заболевания. Сохранение регулярной половой жизни рекомендуется, в общем, всем женщинам и, в частности, женщинам в менопаузе. Это связано с тем, что половой акт улучшает циркуляцию крови во влагалище, и семенная жидкость также содержит половые стероиды, простагландины и незаменимые жирные кислоты, которые способствуют сохранению вагинальной ткани [12].
Хотя официальная распространенность атрофии влагалища меняется в зависимости от численности и индивидуальных особенностей изучаемого населения, все большее число женщин страдают от этого состояния по мере старения населения. Одно из исследований, проведенное зарубежными коллегами, показало, что более 60% женщин испытывают симптомы ВА спустя 4 года после наступления постменопаузы. При этом всего лишь 4% женщин в возрасте 55–65 лет связывают вышеуказанные жалобы с атрофией влагалища, 37% знают, что это симптомы обратимы, и 75% женщин считают, что симптомы ВА негативно влияют на их жизнь. Учитывая деликатный характер этих симптомов, пациентки не решаются обратиться за медицинской помощью и, следовательно, страдают от прогрессирующих симптомов [10, 23]. Лишь 25% женщин с симптомами вагинальной атрофии обращаются за медицинской помощью. ВА является хроническим и прогрессирующим состоянием [10]. Значительное число женщин с симптомами ВА даже не представляют, что существует возможность эффективного лечения. Своевременное информирование пациентов о причинах возникновения вышеуказанных симптомов и возможностях их устранения может позволить в короткие сроки улучшить состояние женщин, возвратить им интерес к жизни и ее качество. Таким образом, проблема сохранения здоровья и профилактики заболеваний, обусловленных старением, приобрела в последние годы особое значение. В связи с ее актуальностью в настоящее время проводится разработка и внедрение новых лекарственных препаратов для лечения ВА, что позволит индивидуализировать подход к лечению пациентов.
Литература
ФГБУ НЦ АГиП им. В. И. Кулакова МЗ РФ, Москва
Abstract. According to forecasts to 2030 there will be 1,2 bln women in postmenopause. The state of oestrogen deficit in climacterical period cause vaginal atrophy with 15–57% of women. The latest data on the problem of pathogenesis, clinical manifestations and therapy of this state are provided in review.
Заместительная гормональная терапия в климактерии
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Научный Центр акушерства, гинекологии и перинаталогии РАМН, Москва
П оскольку в климактерии большинство заболеваний возникает в результате снижения и “выключения” функции яичников, логичным представляется использование заместительной гормональной терапии (ЗГТ). Цель ЗГТ – фармакологически заменить гормональную функцию яичников у женщин, испытывающих дефицит половых гормонов. Важно достичь таких минимально–оптимальных уровней гормонов в крови, при которых реально обеспечивался бы лечебный и профилактический эффект при климактерических расстройствах с минимальными побочными эффектами эстрогенов, особенно в эндометрии и в молочных железах.
Перед решением вопроса о типе ЗГТ врач должен предоставить женщине максимум информации о системном влиянии половых гормонов и их дефицита, а также об эффективности ЗГТ. Это позволяет получить информированное согласие женщины на применение ЗГТ.
В последние годы отмечается тенденция к раннему назначению ЗГТ (в перименопаузе) в следующих случаях:
• ранняя или преждевременная менопауза (38–45 лет)
• длительные периоды вторичной аменореи в репродуктивном возрасте
• первичная аменорея (кроме синдрома Рокитанского–Кюстнера)
• искусственная менопауза (хирургическая, рентген–радиотерапия)
• ранние вазомоторные симптомы климактерического синдрома в перименопаузе
• наличие факторов риска остеопороза и сердечно–сосудистых заболеваний, болезни Альцгеймера.
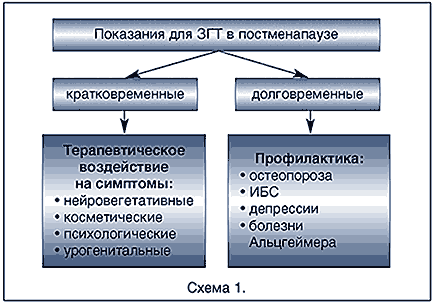
В постменопаузе принято выделять кратковременные и долговременные показания для ЗГТ (схема 1).
Основные принципы применения ЗГТ:
1. Использование лишь “натуральных” эстрогенов и их аналогов, которые значительно слабее синтетических, оказывают минимум побочных эффектов, метаболизируются в организме подобно эндогенным эстрогенам.
1. Использование лишь “натуральных” эстрогенов и их аналогов, которые значительно слабее синтетических, оказывают минимум побочных эффектов, метаболизируются в организме подобно эндогенным эстрогенам.
2. Эстрогены назначаются только в низких дозах, соответствующих уровню эстрогенов в ранней фазе пролиферации менструального цикла молодых здоровых женщин, то есть назначаются минимально оптимальные дозы.
3. Обязательное сочетание эстрогенов с прогестагенами (прогестерон и его аналоги) для защиты эндометрия от гиперпластических процесов.
4. Женщинам с удаленной маткой применяется монотерапия эстрогенными препаратами прерывистыми курсами или в непрерывном режиме.
5. Для обеспечения профилактики поздних метаболических расстройств (остеопороза, ИБС, атеросклероза, болезни Альцгеймера и др.) и лечебного эффекта при мочеполовых расстройствах продолжительность ЗГТ должна составлять минимум 5–7 и более лет.
Существуют следующие основные типы ЗГТ:
• Комбинация эстрогенов с прогестагенами в различных режимах (Климонорм и т.д.)
• Комбинация эстрогенов с андрогенами
• Реже монотерапия прогестагенами или андрогенами.
“Натуральные” эстрогены – это препараты эстрогенов, которые по химической структуре идентичны эстрадиолу, синтезируемому в организме женщин. Благодаря современным технологиям создан синтетический эстрадиол, но по своей химической структуре он идентичен натуральному.
В клинической практике используются следующие препараты эстрогенов:
1. Синтетический “натуральный” эстрадиол–17b.
2. Эстрадиола валерат, который подвергается биотрансформации в печени в эстрадиол.
3. Конъюгированные эстрогены представляют собой так называемые натуральные эстрогены. Они не содержат эстрогенов человека, так как их получают из мочи жеребых кобыл. Поэтому более правильно употреблять термин конъюгированные эквин–эстрогены (КЭЭ).
В течение последних 20–25 лет в Европе доминируют препараты для ЗГТ, содержащие эстрадиол–17b, и эстрадиола валерат. Установлены оптимальные дозы эстрогенных препаратов для лечения типичного климактерического синдрома, для профилактики атеросклероза, остеопороза (табл. 1). Эти же дозы эстрогенов целесообразно назначать и при других показаниях.
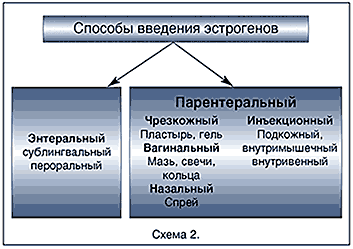
Существуют два основных пути введения эстрогенных препаратов – энтеральный и парэнтеральный (схема 2).
Характеристика оральных эстрогенов:
• простота и удобство в применении
• простота и удобство в применении
• положительное влияние на некоторые показатели липидного спектра крови (снижение общего холестерина; снижение липопротеинов низкой плотности (ЛПНП); повышение липопротеинов высокой плотности (ЛПВП); снижение уровня окисления ЛПНП)
• положительное влияние на обмен в эндотелии сосудов (синтез оксида азота, простациклина и др.), что способствует снижению резистентности сосудов
• возможно неполное всасывание оральных эстрогенов в желудочно–кишечном тракте, особенно при заболеваниях его
• активный метаболизм при прохождении через печень
• повышение концентрации эстрогенов в печени может стимулировать синтез различных биологически активных веществ: факторов свертывания, ангиотензина, глобулина,связывающего половые стероиды, и тироксин–связывающего глобулина
• пациентки иногда не отвечают на оральную ЗГТ, что может быть связано с измененной чувствительностью к незначительным колебаниям уровня эстрадиола или с активным “связыванием” его белками, а также нарушением всасывания его в желудочно–кишечном тракте.
Изложенные факторы могут влиять на фармакокинетику гормональных препаратов, вызывать колебания их уровней в крови. При заболеваниях печени и желудочно–кишечного тракта нарушается всасывание и метаболизм оральных гормональных препаратов. И все же следует отметить, что таблетки – более традиционная форма лекарств для пациентов. Они удобны в применении, дешевле, чем другие формы. И наконец накоплен достаточно длительный опыт их применения.
Парентеральный путь введения преследует основную цель – без потерь доставить лекарственные вещества во внутренние среды организма или непосредственно в патологический очаг. Эстрогены, обладающие липофильностью, могут проникать через кожу, всасываться в кровь и оказывать системное воздействие. Разработаны специальные терапевтические системы для обеспечения чрезкожного поступления лекарственных веществ в системный кровоток.
Показания для парентерального введения эстрогенов для ЗГТ:
• нечувствительность к оральной ЗГТ
• заболевания печения, поджелудочной железы, желудочно–кишечная мальабсорбция
• расстройства коагуляции, тромбоэмболии в анамнезе
• гипертриглицеридемия до– и на фоне оральных, и, особенно, конъюгированных эквинэстрогенов
• повышенный риск холелитиаза
• мигренозные головные боли
• для снижения инсулин–резистентности и улучшения толерантности к глюкозе
• для повышения приемлемости ЗГТ.
Трансдермальное введение эстрогенов позволяет избежать их прохождения через печень и, соответственно, избежать метаболизма в ней. Кроме того, поддерживается сравнительно стабильный уровень эстрадиола в крови без раннего пика, наблюдаемого при оральном приеме.
Пластырь наклеивается, а гель наносится на кожу бедер, живота или ягодиц, поочередно. Степень всасываемости геля зависит от области его нанесения. Установлено, что область бедер более проницаема для геля с эстрадиолом, чем другие области, например, плечо.
Местное вагинальное применение эстрогенов показано при мочеполовых расстройствах. В нашей стране накоплен большой клинический опыт применения препаратов эстриола в виде свечей и мазей. Эстриол обладает выраженным местным кольпотропным эффектом при незначительном системном влиянии на эндометрий.
Для женщин с интактной маткой назначение эстрогенов сочетается с прогестагенами во избежание развития гиперпластических процессов и рака эндометрия.
Термины “прогестагены”, “прогестины”, “гестагены” – синонимы и употребляются для всех стероидов, которые используются в клинической практике с целью замещения эндогенного прогестерона.
Прогестагены добавляются к эстрогенам в циклическом (10–12–14 дней) или в непрерывном режиме. Они могут оказывать побочные метаболические эффекты на липопротеины и углеводный обмен и таким образом частично нивелировать благоприятное влияние эстрогенов на риск сердечно–сосудистых заболеваний.
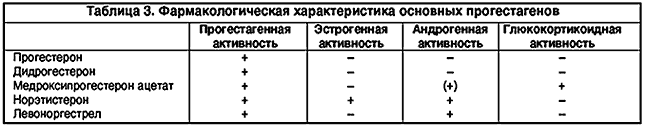
Прогестагены делятся на 2 основные группы (табл. 2):
I –прогестерон и прогестерон–подобные соединения;
II – производные 19–нортестостерона.
Биологические эффекты прогестагенов
Общее основное свойство прогестагенов состоит в способности вызывать секреторную трансформацию пролиферирующего под влиянием эстрогенов эндометрия. Кроме того, прогестагены могут обладать другими эффектами: эстрогенным, антиэстрогенным, андрогенным, антиандрогенным, антигонадотропным, глюкокортикоидоподобным и АКТГ–подобным (табл. 3).
Производные 19–нортестостерона обладают выраженным прогестагенным эффектом, а также антиэстрогенным и андрогенным.
Влияние прогестагенов на эндометрий зависит также от типа, дозы и продолжительности влияния эстрогенов в составе ЗГТ. В таблице 4 представлены оптимальные дозы прогестагенов и длительность их применения для реальной защиты эндометрия.
Эпидемиологические исследования показали, что эстрогены снижают риск инфаркта миокарда на 25–40%. Добавление прогестагенов к эстрогенам, в основном в циклическом режиме, способствует улучшению результатов – снижению риска инфаркта миокарда на 40–50%.
Режимы заместительной гормонотерапии с использованием прогестагенов
Эта терапия назначается женщинам с интактной маткой. Существует два основных режима сочетанной (эстрогены с прогестагенами) ЗГТ:
I – комбинированная терапия (эстрогены с прогестагенами) в циклическом режиме, показана женщинам в перименопаузе (Климонорм, Климен, Цикло–Прогинова)
II – комбинированная терапия (эстрогены с прогестагенами) в монофазном непрерывном режиме.
Основные противопоказания для ЗГТ:
• нелеченый рак молочной железы и эндометрия, опухоли яичников
• почечная и печеночная недостаточность
• острый тромбоз, тромбоэмболия
• менингиома (противопоказаны гестагены)
• маточное кровотечение неясного генеза
• тяжелые формы сахарного диабета.
Обследование перед назначением ЗГТ:
• изучение анамнеза (с учетом вышеперечисленных противопоказаний)
• гинекологическое обследование с онкоцитологией
• УЗИ эндометрия с оценкой толщины эндометрия
• пальпация молочных желез и маммография
• остеоденситометрия в перименопаузе, если имеются факторы риска. Желательно проводить всем женщинам в постменопаузе.
Первый контроль следует назначать через 3 месяца, в последующем – каждые 6 месяцев. Обязательная ежегодная маммография, УЗИ гетиналий, онкоцитология и остеоденситометрия при остеопении и/или остеопорозе.
Следует отметить, что в течение последних 10 лет число противопоказаний уменьшается, а бывшие абсолютные противопоказания к ЗГТ становятся относительными. В значительной степени этому способствовало создание новых форм (парентеральных) препаратов для ЗГТ.
Побочные эффекты ЗГТ: нагрубание молочных желез, снижение или повышение массы тела (у 4–5%), тошнота, пастозность, задержка жидкости, головные боли, обильное выделение цервикальной слизи, холестаз, снижение или повышение либидо. При нагрубании молочных желез лечение не отменяется, а назначается мастодинон или кламин.
Эффективность ЗГТ можно рассмотреть на примере двухфазного препарата Климонорм, т.к. он стал одним из первых препаратов в России, которые применяются для ЗГТ. У большинства отечественных гинекологов уже имеется опыт его применения.
Климонорм – препарат для ЗГТ, который может долгосрочно использоваться там, где не только отдается предпочтение лечению острых климактерических расстройств, но и есть необходимость учесть его благотворное профилактическое действие. Климонорм является подходящим лечебным средством для женщин в перименопаузе, когда еще важно сохранение регулярного менструального цикла. Он может быть также рекомендован женщинам с синдромом истощения яичников, перенесшим операцию овариоэктомии.
Климонорм можно включить в число первоочередных лекарств, которые обеспечат женщине многолетнюю профилактику в климактерии. В результате клинических исследований, проведенных сотрудниками Научного Центра акушерства, гинекологии и перинатологии РАМН, было показано, что Климонорм эффективно снижает частоту и тяжесть климактерического синдрома у женщин в перименопаузе; заместительная гормонотерапия Климонормом не способствует увеличению массы тела и повышению артериального давления; обеспечивает регулярность и стабильность менструального цикла у женщин в перименопаузе, что является реальной профилактикой развития гиперпластических процессов в эндометрии и подтверждено данными ультразвукового мониторинга и гистологическим исследованием эндометрия.
Климонорм не имеет серьезных побочных эффектов и не оказывает негативного влияния на биохимические показатели крови. На фоне терапии отмечается увеличение минеральной плотнотности костей на 2,6% за год.
Профилактическое применение ЗГТ показано при желании женщины получать ЗГТ для улучшения качества жизни, профилактики сердечно–сосудистых заболеваний и остеопороза при отсутствии противопоказаний.
_575.gif)