Кошачий пищевод у человека что
Е. В. Иванова, Н. Н. Щеголева, Л. М. Михалева, З. В. Галкова, Е. Д. Федоров
Научно-образовательный центр абдоминальной хирургии и эндоскопии РГМУ им. Н. И. Пирогова (Зав. — проф. С. Г. Шаповальянц)
ГКБ № 31 (гл. врач член-корр. РАМН, проф. Г. Н. Голухов)
г. Москва
Эозинофильный эзофагит (ЭоЭ) (синонимы: первичный-, аллергический-, идиопатический ЭоЭ) — это воспалительное заболевание пищевода со специфическими клиническими и патоморфологическими проявлениями, характеризующееся плотной эозинофильной инфильтрацией стенки пищевода, с выраженной гиперплазией плоскоклеточного эпителия. В норме в слизистой оболочке пищевода эозинофилы отсутствуют. Их выявление у пациентов с симптомами гастроэзофагеальной рефлюксной болезни (ГЭРБ) ранее, с конца 70-х до середины 90-х годов, относили к ее проявлениям. Однако к 1995 году появилось достаточно данных, чтобы утверждать, что изолированная эозинофильная инфильтрация пищевода может быть проявлением отдельного заболевания [5]. Интерес к проблеме усилился в последние годы; в частности, за последние 5 лет опубликовано более половины всех научных работ посвященных ЭоЭ. На сегодняшний день ЭоЭ считается наиболее частым «эозинофильным заболеванием» желудочно-кишечного тракта. Заболеванию подвержены, как дети, так и взрослые; конкретные цифры его распространенности до конца не ясны [8]. ЭоЭ чаще встречается у мужчин (3:1) и у детей. Вопросы этиологии данного заболевания дискутабельны. Рассматривается роль пищевых и воздушных аллергенов. Также обсуждается возможность аутоиммунного характера заболевания. Считается, что пищевая аллергия при ЭоЭ носит характер пищевой гиперчувствительности и является аллергической реакцией IV типа.
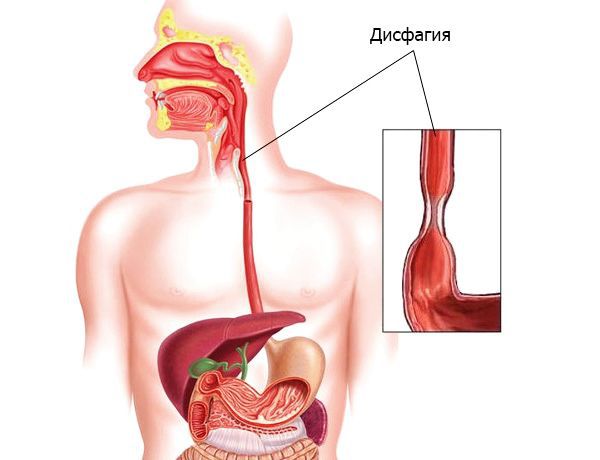
Клиническая диагностика ЭоЭ затруднительна, так как симптомы заболевания подобны таковым при ГЭРБ. Они включают изжогу, срыгивание, рвоту, боль в эпигастрии, дисфагию, ощущение остановки пищевого комка и одинофагию. Симптомы, особенно рвота и дисфагия, чаще носят интермитирующий характер с частотой 1-2 раза в месяц. Изжога и боль в эпигастрии более постоянны. Около 35-45 % пациентов имеют семейный анамнез пищевой аллергии или астмы. Сопутствующий бронхоспазм, экзема или ринит встречается у 45-50 % больных. Важно то, что несмотря на схожесть клинической картины ЭоЭ и ГЭРБ, симптомы и патоморфологические изменения слизистой оболочки пищевода характерные для ЭоЭ не устраняются при приеме медикаментов, подавляющих кислотопродукцию, в том числе при приеме ингибиторов протонной помпы в высоких дозах. Однако исключение специфического пищевого аллергена (ов) способно нивелировать симптомы заболевания. Основные критерии дифференциальной диагностики ЭоЭ и ГЭРБ приведены в таблице 1.
Табл. 1. Дифференциальная диагностика эозинофильного эзофагита и ГЭРБ
| Эозинофильный эзофагит | ГЭРБ |
| Симптомы дисфункции пищевода — интермитирующие | Симптомы — постоянные |
| Нормальные данные рН-метрии | Патологические данные рН-метрии |
| Антисекреторная терапия без эффекта | Антисекреторная терапия эффективна |
| В биоптате слизистой оболочки имеется более 15 эозинофилов в поле зрения | В биоптате слизистой оболочки имеется 1-5 эозинофилов в поле зрения |
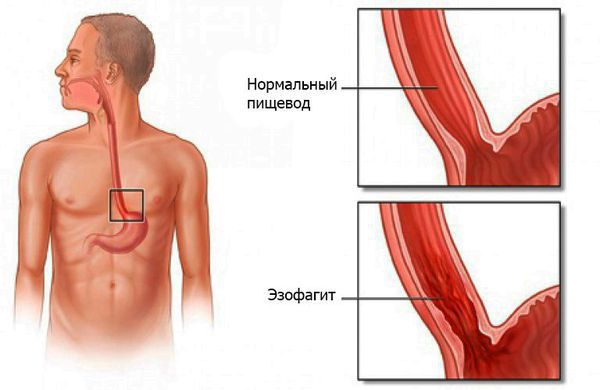
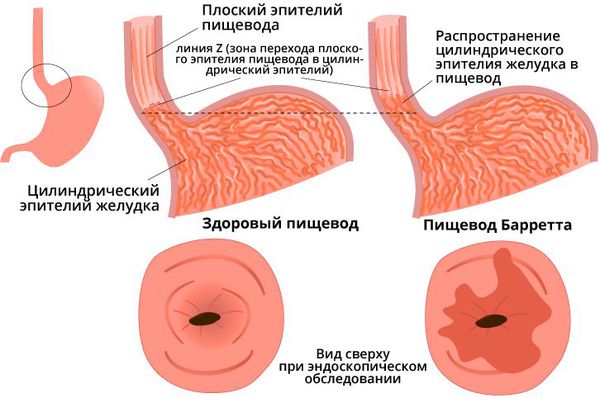
Эндоскопическая картина и эндосонография. ЭоЭ не имеет патогномоничных эндоскопических признаков, хотя часть авторов настаивает на существовании ряда критериев, позволяющих заподозрить эту патологию при выполнении эндоскопии. Основные изменения слизистой оболочки пищевода – множественные циркулярные кольца (трахееподобный вид, «кошачий пищевод»), отек, вертикальные борозды, узловатость, белесые точки или наложения; возможно сужение просвета и наличие стриктур пищевода [1, 6, 7]. Однако специфичность этих признаков невысока, а у 40-50 % пациентов с ЭоЭ эндоскопическая картина соответствует норме. В последнее время появились сообщения, что для эозинофильного эзофагита характерна высокая ранимость слизистой, для ее описания даже был предложен термин — слизистая типа «папиросной бумаги» [10]. В исследовании Fox V. L. с соавт. [3] у 11 детей с эозинофильным эзофагитом было выполнено ультразвуковое исследование пищевода. По данным ЭУС было отмечено значительное утолщение всей стенки пищевода или её отдельных слоёв.
Морфология.
Для ЭоЭ характерна «выраженная» изолированная эозинофильная инфильтрация пищевода. Несмотря на то, что однозначного толкования понятия «выраженная» не достигнуто, большинство авторов соглашается с тем, что наличие более 15-20 эозинофилов в поле зрения является достоверным диагностическим критерием ЭоЭ [8]. Однако, эозинофилия пищевода, правда менее выраженная, встречается не только при ЭоЭ. Она наблюдается и при других заболеваниях, таких как ГЭРБ, болезнь Крона, заболевания соединительной ткани, инфекционный эзофагит (герпес, кандидоз), лекарственно-ассоциированный эзофагит, гиперэозинофильный синдром и эозинофильный гастроэнтерит. Отличительной особенностью ЭоЭ при морфологическом исследовании является выраженная стойкая эозинофилия слизистой оболочки пищевода, зачастую с эозинофильными микро-абсцессами. Слизистая оболочка желудка и двенадцатиперстной кишки при ЭоЭ, как правило, не изменена.
Осложнения, встречающиеся при ЭоЭ.
Считается, что хроническое эозинофильное воспаление является причиной истонченности, ранимости и потери эластичности слизистой оболочкой пищевода. Это, в свою очередь, способно привести к разрывам слизистой в ходе проведения эндоскопического исследования и дилатации пищевода, а также к трансмуральной перфорации при ЭГДС и к разрыву пищевода при вклинении в просвет органа пищевого комка [9]. С учетом этого, сразу несколько авторов призывают к соблюдению осторожности при эндоскопическом лечении сужений и стриктур пищевода, вызванных ЭоЭ. В настоящее время принято считать, что эндоскопическую дилатацию пищевода следует выполнять только у тех пациентов, у которых местная терапия стероидами в течение 8 недель была не эффективной [4].
Лечение.
Терапия при ЭоЭ включает элиминационную диету (исключение из питания аллергогенных групп продуктов — молока, сои, яиц, пшеницы, рыбы, моллюсков и орехов) и применение местных кортикостероидов, таких как флутиказон, будесонид или беклометазон [2]. Рекомендуется два распыления этих препаратов в ротовой полости с последующим проглатыванием два раза в день в течение 6 недель. Единственным описанным осложнением такой терапии является кандидоз пищевода, который наблюдался при применении флyтиказона в дозе 220 мг два раза в день [11]. Кроме того, в лечении используются селективные антагонисты лейкотриенов и препараты, направленные на снижение продукции цитокинов. Антисекреторная терапия и антирефлюксные операции при ЭоЭ не эффективны.
Клинический пример.
Пациент С., 17 лет, обратился в нашу клинику 13.07.2010г. с жалобами на чувство дискомфорта в эпигастрии для проведения диагностической ЭГДС. Позже, при более тщательном сборе анамнеза, мы выяснили, что при аллергической реакции на употребление даже незначительного количества «запрещенных» продуктов или пищи их содержащей, например, орехов, пациент достаточно часто наблюдал тошноту, затруднение прохождения пищи по пищеводу, чувство комка за грудиной. Боли и изжоги его не беспокоили. С первых лет жизни наш пациент страдал выраженной пищевой и лекарственной аллергией, которая проявлялась сыпью на коже, ринитом, отеком Квинке; ранее перенёс анафилактический шок. В детском возрасте часто и длительно, до 6-7 раз в год, болел простудными заболеваниями. В возрасте 4-х лет был поставлен диагноз атопическая бронхиальная астма. По данным результатов общего анализа крови, на протяжении всей жизни, отмечалась эозинофилия. Нами при первичной ЭГДС высокой чёткости и в узком спектре света были выявлены: небольшая хиатальная грыжа; рефлюкс-эзофагит степени В по Лос-Анжелесской классификации; ультракороткий пищевод Барретта (С0М0,8) – единственный «язычок», выстланный эпителием кардиального типа, в т. ч. по данным морфологического исследования; воспалительно-гиперпластические изменения в основании эрозий в зоне пищеводно-желудочного перехода; эндоскопические признаки кандидомикоза пищевода (множественные белесоватые несмываемые бляшки, но без морфологического подтверждения!); Нр-ассоциированный эрозивный антрум-гастрит и эрозивный бульбит. Было проведено лечение (нексиум, де-нол, вильпрофен, флемоксин, мотилиум, флуконазол). При повторном осмотре через 3 месяца (19.10.2010г.) жалоб нет. На фоне полной эпителизации эрозий пищевода и желудка нами было отмечено наличие характерных признаков эозинофильного эзофагита: «кошачий» пищевод (Рис.1), отек слизистой, вертикальные борозды (Рис. 2), множественные белесые наложения (Рис. 3), которые ранее расценивались как проявления кандидозной инфекции.
Для более точной верификации диагноза 28.12.2010г. мы выполнили пациенту ЭУС и повторную множественную щипцовую биопсию слизистой оболочки пищевода. При ЭУС выраженного утолщения стенки пищевода выявлено не было, однако отмечалась некоторая смазанность слизистого и подслизистого слоев (Рис. 4). По данным морфологического исследования выявлена выраженная эозинофильная инфильтрация в слизистом и подслизистом слоях: от 10 до 80 эозинофилов в поле зрения, при ув. х360 (Рис. 5, 6). При этом наличия мицелл грибка Candida albicans обнаружено не было (!), несмотря на то, что при этом предновогоднем исследовании размеры и количество несмываемых бляшек увеличилось и внешне они выглядели, как кандидомикоз пищевода. Подобные белесоватые наложения, судя по данным литературы и нашим находкам служат проявлением эозинофильных микроабсцессов.
Таким образом, по совокупности клинических и инструментальных находок, пройдя этап недиагностированного заболевания, а затем этап клинических, эндоскопических и морфологических сомнений, в конечном итоге пациенту был установлен диагноз эозинофильный эзофагит. В настоящий момент консилиумом с «семейным» иммунологом и гастроэнтерологом обсуждается тактика ведения и подбирается оптимальное лечения нашего пациента.
Эозинофильный эзофагит
Эозинофильный эзофагит (англ. eosinophilic esophagitis; EoE) — клиническая форма поражения пищевода, развивающаяся на фоне аутоимунных заболеваний. Характеризуется увеличенным количеством эозинофилов в слизистой оболочке пищевода (эозинофилы — один из видов лейкоцитов крови). Предполагают, что причиной такой формы эзофагита является пищевая или респираторная аллергия и она требует иной тактики лечения, отличной от рефлюкс-эзофагита.
Эозинофильный эзофагит имеет тенденцию к увеличению частоты. В США в настоящее время зафиксировано 150 000 больных эозинофильным эзофагитом, 75 % из которых — взрослые.
Эозинофильный эзофагит является распространенной причиной рефрактерной терапии к гастроэзофагельной рефлюксной болезни (ГЭРБ). Пациенты с эозинофильным эзофагитом обычно молодые люди, имеющие в анамнезе указания на перемежающуюся дисфагию, появляющуюся после приёма твердой пищи, и часто — на задержку пищи в пищеводе. Довольно частым ошибочным диагнозом при наличии эзофагита у этих больных является ГЭРБ. У многих больных имеется связь с развитием астмы или наличием пищевой аллергии, особенно против молока, яиц, арахиса или дынь. На предполагаемый диагноз эозинофильного эзофагита указывают эндоскопические проявления: множественные кольца в просвете пищевода, продольные бороздки, или экссудат белого цвета (Пасечников В.Д.).

Гистологическое исследование биоптата. Гиперплазия клеток базального слоя многослойного плоского эпителия (а). Эозинофилы в межклеточных пространствах – более 20 в 1 поле высокого разрешения в многослойном плоском эпителии пищевода (б). Окраска гематоксилином и эозином. Увел. а) х120, б) х500 (Валитова Э.Р. и др.).
При биопсии проксимального и дистального отделов пищевода в гистологических препаратах определяются более 15-20 эозинофилов в поле зрения.
Эозинофильный абсцесс в слизистой оболочке пищевода. Furuta G. et al, Gastroenterology, 2007; 133: 1342-1363.
Периферическая эозинофилия не является распространенным патологическим признаком. Патогенез эозинофильного эзофагита не известен. Предполагают, что развитие этого состояния провоцируется приемом пищи и аэроаллергенов, стимулирующих ответ цитокинов, обусловленных активацией Т-хелперов 2 типа, другие исследования предполагают, что у некоторых пациентов имеется атипичный вариант ГЭРБ. Естественное течение эозинофильного эзофагита плохо изучено, но известно, что оно не связано с исходом в рак пищевода. Симптомы этого заболевания и снижение количества эозинофилов в ткани достигается после трёхмесячного назначения ингаляционных стероидов (флутиказона пропионата дважды в день утром и вечером по 440 мкг). Для гарантированного адекватного поступления стероидов в пищевод, а не в легкие, спейсер не должен использоваться вместе с ингалятором. В случае, если ингаляционные стероиды не приводят к разрешению симптомов, используется иная терапия, включающая применение антагониста лейкотриена D4 (монтелюкаста 10-40 мг в день) или пероральных стероидов (преднизон 30 мг в день в течение 2 недель) с постепенным снижением дозы в течение 6 недель. У других пациентов используются ингибиторы протонной помпы с последующим бужированием стриктур (Пасечников В.Д.).
Имеются исследования, доказывающие, что после исключения из рациона больных шести групп наиболее вероятных аллергенов (молочные продукты, соя, пшеница, орехи, морепродукты, яйца) у большинства отмечаются клинические, эндоскопические и гистологические улучшения (Wolf WA et al, Clin Gastroenterol Hepatol. 2014;12:1272-1279).
Лечение эозинофильного эзофагита
Ингибиторы протонной помпы 20–40 мг (в зависимости от выбранного препарата) 1–2 раза в день в течение 8–12 недель или 1 мг/кг на 1 прием дважды в день в течение 8–12 недель у детей значительно облегчают симптомы и приводит к нормализации гистологической картины у значительной группы пациентов.
Системное применение кортикостероидов имеет строгие показания: тяжелая дисфагия как результат осложнений эозинофильного эзофагита (стриктуры и узкий пищевод); связанная с осложнениями госпитализация; потеря массы тела. Из-за значительных побочных эффектов длительное применение системных стероидов при эозинофильном эзофагите не рекомендовано.
Топические стероиды применяют у детей и взрослых для индукции ремиссии и поддерживающей терапии. Они хорошо переносимы и имеют минимальные побочные эффекты, среди которых наиболее частыми являются кандидоз полости рта и пищевода, герпетическая инфекция. Для индукции ремиссии применяют флутиказон в дозе 440–880 мкг дважды в день по схеме впрыск–глоток и будесонид (густая суспензия) 2 мг в день. После приема топических стероидов не рекомендуется принимать пищу и пить в течение 30 минут. После успешной индукции ремиссии необходима длительная поддерживающая терапия.
Раздел «Лечение. » написан на основе статьи Ивашкина В.Т. и др.
Что такое эзофагит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Аверин А. А., эндоскописта со стажем в 12 лет.
Определение болезни. Причины заболевания
Эзофагит — воспаление слизистой оболочки пищевода, возникающее под действием инфекций, химических веществ, физических факторов и генетической предрасположенности.
Выделяют три формы эзофагита:
Эзофагит развивается под влиянием внешних и внутренних причин.
Внешние причины воспаления слизистой оболочки пищевода:
1. Инфекционные — воздействие патогенных микробов, например грибов рода Candida и герпесвирусов. Инфекционная форма эзофагита преобладает у людей с иммунодефицитом, но необязательно вызванного ВИЧ-инфекцией. Также высокий риск развития заболевания у пациентов, длительно принимающих стероиды при бронхиальной астме и хронической обструктивной болезни лёгких.
2. Химические — влияние агрессивных веществ (кислот или щелочей) и некоторых лекарственных средств:
3. Физические — факторы окружающей среды, такие как температура, излучение, механическое воздействие:
Внутренние причины эзофагита:
Вышеперечисленные факторы приводят к воспалению слизистой оболочки пищевода. В зависимости от интенсивности и продолжительности процесса оно протекает или остро, приводя к развитию острого эзофагита, или длительно, вызывая хроническую форму болезни.
Симптомы эзофагита
Симптомы заболевания различны в зависимости от вида эзофагита. Самый распространённый тип данного заболевания — рефлюкс-эзофагит.
К основным симптомам рефлюкс-эзофагита относятся:
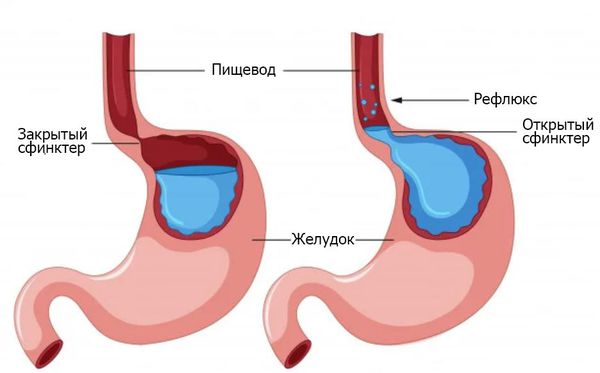
Рефлюск-эзофагит — один из вариантов течения гастроэзофагеальной рефлюксной болезни (ГЭРБ) с воспалением пищевода. В основе ГЭРБ лежит нарушение моторной функции нижнего пищеводного сфинктера и постоянные забросы кислого содержимого желудка в пищевод. Симптомы заболевания делятся на пищеводные и внепищеводные.
Пищеводные симптомы ГЭРБ:
Внепищеводные проявления ГЭРБ:
Основные симптомы инфекционного эзофагита:
Вышеописанные симптомы часто сочетаются с лихорадкой, сепсисом, анорексией и потерей веса. Иногда пациентов беспокоит кашель.
При развитии осложнений добавляются новые симптомы:
Симптомы хронического эзофагита
Все описанные симптомы характерны как для острого, так и для хронического эзофагита. Разница между ними в выраженности и продолжительности болезни:
В дальнейшем при хроническом эзофагите периоды обострения чередуются с ремиссией.
Патогенез эзофагита
Различные формы эзофагита отличаются причинами, вызвавшими заболевание, и механизмами развития воспаления в слизистой оболочке пищевода.
Рефлюкс-эзофагит
Рефлюск-эзофагит — один из вариантов течения гастроэзофагеальной рефлюксной болезни (ГЭРБ) с развитием воспаления пищевода. Патогенез рефлюкс-эзофагита:
Инфекционный эзофагит
Эозинофильный эзофагит
Эозинофильный эзофагит развивается следующим образом:
Классификация и стадии развития эзофагита
В Международной классификации болезней (МКБ-10) эзофагит кодируется как К20.
По этиологии:
По характеру поражения:
По распространённости:
По локализации:
По течению:
По периодам болезни:
По клиническим проявлениям:
По осложнениям:
В клинической практике наиболее распространены две эндоскопические классификации для хронической и острой формы эзофагита.
Классификация H. Basset различает четыре степени острого эзофагита [3] :
В зависимости от выраженности поражения стенки пищевода хронический эзофагит делят на четыре степени (классификация Савари — Миллера) [9] :
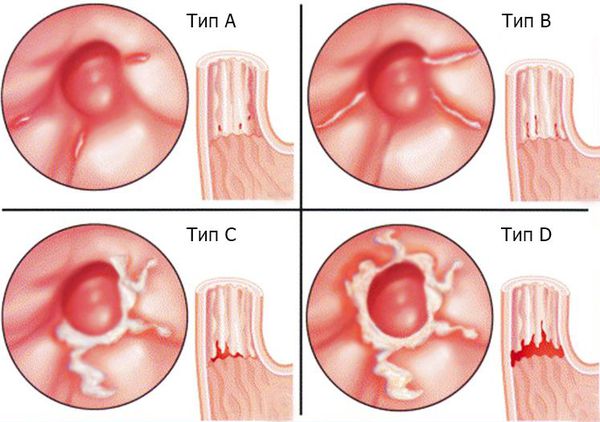
При рефлюкс-эзофагите (ГЭРБ) используется Лос-Анджелесская классификация [4] :
Стадии эзофагита:
Стадии повторяются и приводят к развитию осложнений.
Осложнения эзофагита
При длительном течении хронического эзофагита (чаще при рефлюкс-эзофагите) развиваются следующие осложнения:
Одним из наиболее опасных осложнений эзофагита является развитие рака пищевода — аденокарциномы.
Диагностика эзофагита
Общий осмотр пациента не даёт результатов, так как эзофагит не имеет внешних проявлений. Лабораторные методы также неинформативны, они помогут только выявить осложнение заболевания — кровотечения из верхних отделов желудочно-кишечного тракта. При подозрении на иммуносупрессию пациенты сдают развёрнутый клинический анализ крови и тесты на ВИЧ.
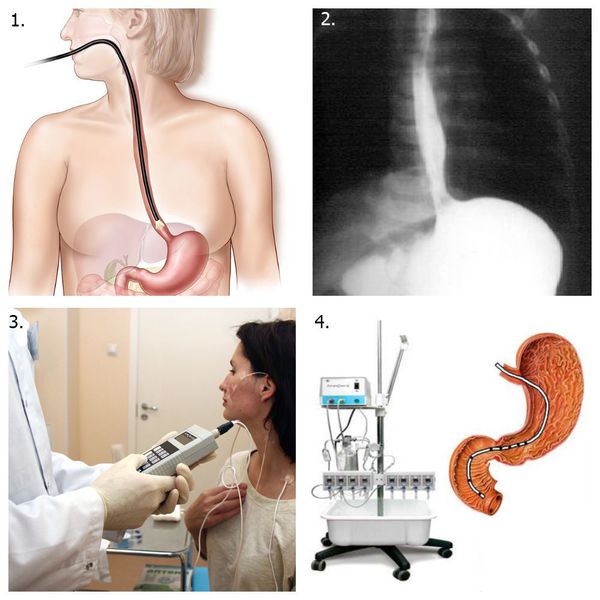
Для диагностики эзофагита применяют инструментальные методы:
Вспомогательные методы:
Ведущими методами диагностики является ЭГДС и рентгенологическое исследование пищевода. При этом рентгенографическое исследование пищевода с барием и эндоскопия верхних отделов ЖКТ дополняют друг друга, а не конкурируют.
Лечение эзофагита
Лечение эзофагита зависит от типа и причины заболевания. Чаще применяется медикаментозная терапия.
Консервативное лечение
Лечение рефлюкс-эзофагита:
При лекарственном эзофагите — отмена препарата или замена на лекарства без побочных эффектов. Таблетки следует запивать не менее чем 100-150 мл воды и оставаться в вертикальном положении 30 минут после их приёма.
При лечении эозинофильного эзофагита и подозрении на пищевую аллергию последовательно исключают различные продукты питания — потенциальные аллергены.
Лечение инфекционного эзофагита направлено на подавление возбудителя и зависит от его природы (грибы, бактерии, вирусы):
Лечение других типов эзофагита зависит от основного заболевания, которое привело к патологии. Распространённые варианты лечения:
Диета
При эзофагите нежелательно употреблять жирную и острую пищу, кофе, газировку, шоколад, горячие напитки и блюда с температурой более 40 °С.
Хирургическое лечение
Операции при эзофагите, как правило, не проводятся. Их выполняют, только если не помогло медикаментозное лечение и развились осложнения.
К таким операциям относятся:
При метастатическом раке пищевода с эзофагитом применяется лучевая терапия в сочетании с паллиативным стентированием.
Прогноз. Профилактика
При своевременной диагностике и правильном лечении прогноз положительный, но на него влияет тяжесть основного заболевания и развитие осложнений.
При появлении осложнений прогноз становится неблагоприятным. Пищевод Барретта является предраковым состоянием и приводит к аденокарциноме пищевода. При развитии стенозов и стриктур пищевода поступление пищи в желудок нарушается, что вызывает истощение и потерю веса с исходом в гипотрофию.
При тяжёлых формах эзофагита могут развиваться такие осложнения, как кровотечение и перфорация. Прогноз при этом крайне неблагоприятный, возможен летальный исход.
Профилактика эзофагита сводится к исключению или ограничению факторов, повреждающих слизистую оболочку пищевода.
Изменения образа жизни и питания — важные составляющие лечения и профилактики эзофагита [12] :
Эозинофильный эзофагит
Общая информация
Краткое описание
Клинические рекомендации по диагностике и лечению эозинофильного эзофагита (Москва, 2013)
Этиология и патогенез
В формировании ЭоЭ имеет значение патогенетическое влияние трех групп факторов: воздействие воздушных и пищевых аллергенов, генетическая предрасположенностьи активация Т-хелперов 2 типа (Th2).
Триггерным фактором развития эзофагита являются аллергены внешней среды (пищевые и воздушные), которые, попадая на слизистую оболочку пищевода, инициируют развитие иммуновоспалительного процесса. Роль пищевых аллергенов в развитии заболевания подтверждается высокой эффективностью элиминационных диет у детей с ЭоЭ.
Для заболевания характерно сезонное течение, с обострением клинической картины и увеличением количества эозинофилов в слизистой пищевода в период цветения растений, что свидетельствует о роли воздушных аллергенов в патогенезе ЭоЭ.
ЭоЭ очень часто протекает на фоне других атопических заболеваний. В целом, до 86% взрослых и 93% детей, больных ЭоЭ, имеют аллергические заболевания на момент обращения, около половины больных отмечают наличие таких заболеваний в анамнезе, что свидетельствует об атопическом характере ЭоЭ.
Итак, пищевые и воздушные антигены являются пусковым фактором заболевания, в основе же патогенеза ЭоЭ лежит генетически детерминированная патология иммунного ответа. Зачастую заболевание носит семейный характер: около 8% больных детей имеют кровных родственников, страдающих ЭоЭ.
На сегодняшний день уже известно несколько генетических аномалий, приводящих к развитию эозинофильной инфильтрации слизистой оболочки пищевода. Усилия ученых направлены на расшифровку новых генов, ответственных за развитие атопических заболеваний в целом и эозинофильного эзофагита в частности.
Возникновение эозинофильного эзофагита обусловлено мутацией в гене TSLP (расположен в хромосоме 5q22), кодирующем синтез тимического стромального лимфопоэтина, а также мутацией в гене, кодирующем синтез рецептора к тимическому стромальному лимфопоэтину (TSLPR), расположенному в половых хромосомах Xp22.3 и Yp11, с чем связано преобладание лиц мужского пола среди больных ЭоЭ. Данная мутация приводит к гиперэкспрессии гена TSLP в слизистой оболочке пищевода.
TSLP является цитокином, экспрессируемым клетками тимуса, слизистой оболочки желудочно-кишечного тракта, легких, кожи. TSLP активирует иммунокомпетентные клетки, в частности, дендритные клетки и мастоциты, способствуя детерминации иммунного ответа по Тh2-зависимому пути. Гиперэкспрессия TSLP характерна не только для ЭоЭ, но и для бронхиальной астмы, атопического дерматита, экземы. Более того, в коже при атопическом дерматите и в слизистой пищевода при ЭоЭ имеются схожие морфологические особенности: эозинофильная инфильтрация и гиперплазия базального слоя многослойного эпителия, дегрануляция эозинофилов, что говорит об общности патогенеза ЭоЭ и атопических заболеваний.
Кроме того, у больных ЭоЭ в гене, кодирующем эотаксин- 3 (аллель G SNP (T/G +2496), 3’ UTR гена эотаксина-3) имеется замена тимина на гуанин в положении 2496, что приводит к гиперэкспрессии цитокина эотаксина – 3.
Эотаксин-3 является хемокином эозинофилов, стимулирующим пролиферацию эозинофилов в костном мозге, выход их в периферическое кровеносное русло. Эотаксин-3 удлиняет время жизни эозинофилов и вызывает их хемоаттракцию в слизистую пищевода. Экспрессия эотаксина-3 в слизистой оболочке пищевода больных ЭоЭ в 50 раз превышает таковую у здоровых добровольцев. Причем, чем выше уровень экспрессии эотаксина-3, тем выраженнее степень воспалительной инфильтрации пищевода.
Таким образом, имеющиеся поломки в генетическом аппарате иммунокомпетентных клеток приводят к развитию иммунного ответа по пути активизации Т-хелперов 2 типа, которые продуцируют чрезвычайно активную группу интерлейкинов (ИЛ-4, ИЛ-5, ИЛ-13), обладающих огромным разнообразием эффектов.
В целом, иммунный ответ при ЭоЭ характеризуется гиперпродукцией Тh2-ассоциированных цитокинов в ответ на воздействие пищевых и воздушных антигенов, что, как известно, характерно для большинства атопических заболеваний. На сегодняшний день ЭоЭ признается одним из проявлений общей атопической реакции организма (наряду с атопическим дерматитом, астмой, пищевой аллергией и другими атопическими заболеваниями). В этой связи всем больным с подозрением на ЭоЭ рекомендовано проведение дополнительных исследований (консультация пульмонолога, исследование функции внешнего дыхания, кожные аллергические пробы и др.), направленных на диагностику бронхиальной астмы, пищевой аллергии и других атопических состояний.
Таким образом, с учетом накопленных на сегодняшний день данных, этиопатогенез ЭоЭ представляется следующим образом: при воздействии воздушных и пищевых аллергенов на слизистую оболочку пищевода у лиц с имеющейся генетической предрасположенностью происходит активация антигенпрезентирующих клеток с последующим представлением антигенов Т-лимфоцитам и мастоцитам. Т-лимфоциты в условиях гиперэкспрессии TSLP детерминируются по пути преимущественного образования Т-хелперов 2 типа и совместно с мастоцитами начинают продуцировать интерлейкины ИЛ-4, ИЛ-5, ИЛ-13, которые, воздействуя на эпителий пищевода, фибробласты, гладкомышечные клетки стимулируют экспрессию ими эотаксина-3.
Гиперпродукция эотаксина-3 эпителиоцитами в результате мутации и/или сенсибилизации вызывает хемоаттракцию эозинофилов в слизистую оболочку пищевода. Кроме того, интерлейкины Т-лимфоцитов 2 типа, особенно ИЛ-5, сами обладают свойствами колониестимулирующих факторов для эозинофилов, активируя их пролиферацию в костном мозге и выход в периферическое русло, увеличивают продолжительность жизни и хемоаттракцию эозинофилов в слизистую пищевода.
Воспаление, индуцированное эозинофилами, характеризуется гиперэкспрессией ИЛ-13 и TGF-ß, которые стимулируют клеточную пролиферацию, фиброзо- и ангионеогенез. Кроме того, эозинофилы синтезируют лейкотриены C4, D4, T4, эффект которых реализуется в повышении сосудистой проницаемости, гиперпродукции слизи, стимуляции сокращений гладкомышечных клеток.
Кроме эозинофилов в слизистой оболочке пищевода больных ЭоЭ наблюдается значительное увеличение числа мастоцитов, присутствующих в здоровом пищеводе в единичных количествах. На поверхности мастоцитов при ЭоЭ обнаруживаются синтезированные (системно или локально) IgE, содействующие активизации тучных клеток пищевыми антигенами. Активированные мастоциты способны высвобождать такие медиаторы воспаления, как цитокины, гистамин, протеазы.
В слизистой оболочке больных ЭоЭ обнаруживаются также В-лимфоциты, продуцирующие IgЕ, высок уровень других субпопуляций лимфоцитов (CD3+,CD8+,CD4+). Массивное повреждение слизистой оболочки иммунокомпетентными клетками быстро приводит к вовлечению в процесс фибробластов и эндотелиоцитов, происходит гиперплазия базального слоя эпителия и гладкомышечных клеток, активация фиброзогенеза и ангионеогенеза в подслизистом слое, что в конечном итоге приводит к потере эластичности мышечной ткани и образованию стриктур стенки пищевода.
Существует влияние еще одного фактора, вносящего значительный вклад в развитие и прогрессирование воспаления слизистой пищевода при ЭоЭ. Речь идет о сопутствующей гастроэзофагеальной рефлюксной болезни.
ГЭРБ служит кофактором в патогенезе ЭоЭ, способствуя более глубокому проникновению антигенов через поврежденную кислотно-пептическим рефлюктатом слизистую пищевода. Наличие кислого рефлюкса усиливает степень эозинофильной инфильтрации слизистой пищевода, способствует высвобождению мастоцитами медиаторов воспаления, а расширение межклеточных пространств при ГЭРБ приводит к взаимодействию антигенпрезентирующих клеток с аллергенами. Поэтому значительная доля пациентов с клиническими и гистопатологическими особенностями, характерными для ЭоЭ, отвечает на антисекреторную терапию клиническим улучшением и уменьшением степени эозинофильной инфильтрации слизистой пищевода.