Клиника «Центр ЭКО»
Бесплодным считается брак, в котором отсутствует беременность у женщины при регулярной половой жизни партнеров без использования каких-либо противозачаточных средств. Ошибочно полагается, что бесплодие относится только к женщинам. В 45 процентах случаев это патология со стороны женщин, а в 40 процентах – у мужчин. Еще в 5-10 процентах случаев нарушения обнаруживаются сразу у обоих партнеров.
Клиническое бесплодие бывает:
Наиболее распространены следующие формы бесплодия:
В клинике бесплодия первой жалобой пациентов является отсутствие беременности либо выкидыши с невозможностью выносить и родить малыша. Также выявляются жалобы, связанные с первичной или сопутствующей патологией. Анамнез также подтверждает нарушения менструального цикла, перенесенные операции и аборты, воспалительные заболевания, или заболевания щитовидной железы, надпочечников, либо травму головного мозга. При физикальном обследовании могут выявиться ожирение, клиника синдрома Иценко-Кушинга, который также провоцирует бесплодие, признаки гиперандрогении (повышение андрогенов – мужских половых гормонов), либо нервная анорексия, клинически также приводящая к бесплодию.
Почему стоит выбрать клинику «Центр ЭКО»?
Преимущества клиники «Центр ЭКО»:
Комфорт и удобство клиники «Центр ЭКО»
Подробно узнать о ВРТ-программах клиники «Центр ЭКО» вы можете в разделе «Наши услуги».
Мы поможем вам осуществить вашу мечту о детях!
Синдром кошачьего крика
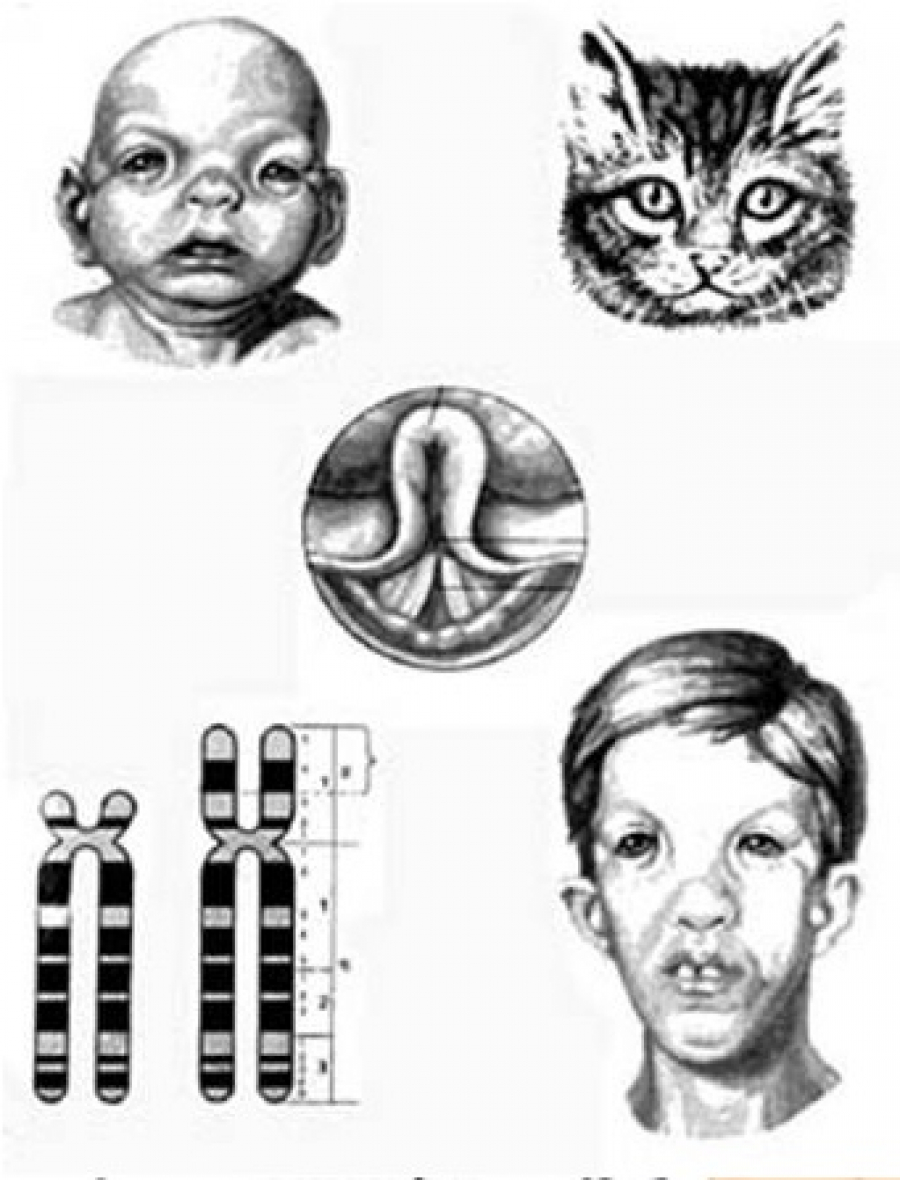
Синдром «кошачьего крика» – хромосомное нарушение, обусловленное делецией (отсутствием) фрагмента короткого плеча 5-ой хромосомы. Плач новорожденных с синдромом «кошачьего крика» по звуку напоминает кошачье мяуканье, что и послужило названию патологии. Кроме этого, у детей имеет место микроцефалия, лунообразное лицо, косоглазие, аномалии прикуса, различные врожденные пороки, грубое интеллектуальное недоразвитие и т. д. Синдром «кошачьего крика» диагностируется на основании совокупности характерных признаков и цитогенетического исследования. Специфического лечения синдрома «кошачьего крика» не существует; дети могут нуждаться в хирургической коррекции тяжелых врожденных аномалий.
Общие сведения
Причины синдрома «кошачьего крика»
Развитие синдрома «кошачьего крика» связано с потерей фрагмента 5-ой хромосомы, а, следовательно, генетической информации, хранящейся на этом участке. В 85-90% случаев делеция короткого плеча образуется в результате случайной мутации, в 10-15% наследуется от родителей, являющихся носителями сбалансированной транслокации.
Наиболее частыми цитогенетическими вариантами хромосомной аберрации служат утрата одной трети или половины длины короткого плеча 5-ой хромосомы. Потеря меньшего участка или всего плеча встречается исключительно редко. При этом для степени выраженности клинической картины синдрома «кошачьего крика» важен не размер утерянного фрагмента, а отсутствие конкретного участка хромосомы. Так, при потере небольшого участка хромосомы в области 5p15.2 развиваются все клинические признаки синдрома, кроме кошачьего крика; критическим для возникновения характерного крика является выпадение участка хромосомы в области 5p15.3.
Наряду с простой делецией, могут встречаться другие цитогенетические вариации синдрома «кошачьего крика»: мозаицизм, кольцевая 5-я хромосома с делецией участка короткого плеча, реципрокная транслокация короткого плеча 5-ой хромосомы на другую хромосому.
Симптомы синдрома «кошачьего крика»
Новорожденные с синдромом «кошачьего крика», как правило, рождаются доношенными, но с небольшой пренатальной гипотрофией (средняя масса при рождении около 2500 г). Беременность у матери может протекать абсолютно нормально или сопровождаться угрозой самопроизвольного прерывания не чаще, чем в популяции. Наиболее патогномоничным ранним признаком синдрома является плач ребенка, который напоминает мяуканье кошки. Высокое и пронзительное звучание детского крика обусловлено анатомическими особенностями строения гортани при данном синдроме – узостью ее просвета, небольшим надгортанником, необычной складчатостью слизистой оболочки, мягкой консистенцией хрящей. Некоторые авторы считают, что специфический крик имеет центральное происхождение и не связан с недоразвитием гортани. Примерно у трети детей «кошачий крик» исчезает к 2-м годам, у остальных остается на всю жизнь.
Фенотип детей с синдромом «кошачьего крика» отличается преобладанием лицевой части черепа над мозговой, лунообразным лицом, гипертелоризмом, антимонголоидным разрезом глаз, эпикантом, деформацией ушных раковин, плоской спинкой носа, короткой шеей с крыловидными складками. При обследовании у детей выявляется микроцефалия, мышечная гипотония, снижение рефлексов, нарушение сосания и глотания. В неонатальном периоде может развиваться инспираторный стридор и цианоз.
Другие клинические проявления синдрома «кошачьего крика» могут значительно варьироваться по своему сочетанию у отдельных больных. Со стороны зрительной системы нередко обнаруживается врожденная катаракта, близорукость, косоглазие, атрофия зрительного нерва. Изменения со стороны костно-мышечной системы проявляются синдактилией стоп, врожденным вывихом бедра, косолапостью, плоскостопием, клинодактилией V пальца кисти, сколиозом, диастазом прямых мышц живота, паховыми и пупочными грыжами. Частыми спутниками синдрома «кошачьего крика» являются нарушения прикуса, «готическое» нёбо, микрогения, расщелины нёба и верхней губы, расщепление язычка.
У многих пациентов наблюдаются врожденные пороки сердца (ДМЖП, ДМПП, открытый артериальный поток, тетрада Фалло), пороки развития почек (гидронефроз, подковообразная почка), крипторхизм, гипоспадия. Реже отмечается мегаколон, запоры, кишечная непроходимость. Дерматоглифическими признаками синдрома «кошачьего крика» могут служить одна ладонная складка, поперечные складки сгибания и др.
Поведение детей характеризуется гиперактивностью, однообразными движениями, склонностью к агрессии и истерикам. Детям с синдромом «кошачьего крика» свойственна глубокая умственная отсталость в степени имбецильности и идиотии, грубое системное недоразвитие речи, выраженное отставание в моторном и физическом развитии.
Половая и репродуктивная функции у лиц с синдромом «кошачьего крика» обычно не страдают. Иногда у женщин выявляется двурогая матка, у мужчин – уменьшение размеров тестикул, однако сперматогенез существенно не нарушен, как, например, при синдроме Клайнфельтера.
Продолжительность жизни больных с синдромом «кошачьего крика» значительно укорочена; большая часть детей погибает в первый год жизни из-за сопутствующих пороков и их осложнений (чаще от сердечной и почечной недостаточности). Лишь около 10% доживают до подросткового возраста, хотя имеются отдельные сообщения о больных, достигших 50 лет.
Диагностика синдрома «кошачьего крика»
Если в семье уже имелись случаи хромосомных заболеваний, еще на этапе планирования беременности будущим родителям рекомендуется посетить генетика и пройти генетическое тестирование. В процессе беременности наличие у плода синдрома «кошачьего крика» может быть заподозрено на основании результатов ультразвукового пренатального скрининга. В этом случае для окончательного подтверждения хромосомной аномалии рекомендуется проведение инвазивной пренатальной диагностики (амниоцентеза, биопсии ворсин хориона или кордоцентеза) и непосредственного анализа генетического материала плода.
После рождения предварительный диагноз синдрома «кошачьего крика» устанавливается неонатологом на основании типичных диагностических признаков (характерного плача, фенотипических черт, множественных стигм дизэмбриогенеза). Для подтверждения хромосомной патологии проводится цитогенетическое исследование.
Учитывая наличие у детей с синдромом «кошачьего крика» множественных аномалий развития, необходимо, чтобы в первые дни жизни новорожденные были осмотрены детским кардиологом, детским офтальмологом, детским урологом, детским ортопедом и другими специалистами.
Лечение синдрома «кошачьего крика»
Специфического лечения данного хромосомного заболевания в настоящее время не существует. Для стимуляции психомоторного развития под наблюдением детского невролога проводятся курсы медикаментозной терапии, массажа, физиотерапии, ЛФК. Дети с синдромом «кошачьего крика» нуждаются в помощи психологов, дефектологов, логопедов.
Врожденные пороки сердца при синдроме «кошачьего крика» часто требуют хирургической коррекции, поэтому детям необходима консультация кардиохирурга, проведение ЭхоКГ и других необходимых исследований. Дети с патологией мочевыделительной системы должны находиться под наблюдением детского нефролога и периодически проходить комплекс необходимых обследований (УЗИ почек, общий анализ мочи, биохимическое исследование крови и мочи и др.).
Прогноз и профилактика синдрома «кошачьего крика»
На продолжительность и качество жизни больных влияет тяжесть самого синдрома и сопутствующих врожденных пороков, уровень оказания медицинской и психолого-педагогической помощи. В целом долговременный прогноз неблагоприятный. При специальном обучении дети имеют словарный запас, достаточный для бытового общения, однако по уровню психомоторного развития обычно не поднимаются выше дошкольников.
Профилактика синдрома «кошачьего крика» заключается в тщательной подготовке к беременности и исключении возможных неблагоприятных воздействий на организм родителей еще задолго до зачатия. При рождении в семье ребенка с синдромом «кошачьего крика», родители в обязательном порядке должны пройти цитогенетическое обследование для исключения носительства реципрокной сбалансированной транслокации.
Синдром «Кошачьего крика» у детей
Развитие современной медицины затрагивают серьезные вопросы, связанные с диагностикой генетических заболеваний.
Мы часто рассказываем о распространенных синдромах, таких как синдром Дауна, Эдвардса, Патау. Однако существуют количественные или качественные изменения генетического материала частота встречаемости которых намного реже, чем трисомия по 21 хромосоме. На сегодняшний день известно около 6 тысяч наследственных генетических заболеваний.
Мы решили завести новую рубрику о генетических заболеваниях, где будем рассказывать о частоте встречаемости, характерных признаках и симптомах.
Синдром «кошачьего крика» 46,ХХ,del5p
Хромосомная патология, связанная с делецией (отсутствием) фрагмента короткого плеча 5-ой хромосомы.
Достаточно редкое заболевание, частота встречаемости 1 на 50000 новорожденных. Данная патология чаще встречается у девочек.
трудности с проглатыванием пищи;
низкий вес при рождении;
задержка в физическом развитии,
неконтролируемое и чрезмерное слюноотделение.
Данного синдрома во время беременности может быть диагностирован при проведении ультразвукового исследования, для подтверждения диагноза назначают инвазивную процедуру.
Несмотря на то, что каждый случай индивидуален. В 90% случаев дети с данной патологией не доживают до 10 лет.
ООО «Медикал Геномикс» Лицензия № ЛО-69-01-002086 от 06.10.2017
Юр. адрес: г. Тверь, ул. Желябова, 48
ООО «Лаб-Трейдинг», ИНН: 6950225035, ОГРН: 1186952017053, КПП:695001001
Юр. адрес: г. Тверь, ул. 1-Я За Линией Октябрьской Ж/Д, 2, оф. 22
Синдром кошачьего крика
Синдром «кошачьего крика» впервые описал Ж. Лежен с соавторами в 1963 г. у 3 детей с множественными аномалиями, глубокой умственной отсталостью и характерным плачем, который напоминал кошачий крик.
Клинически синдром «кошачьего крика» очень полиморфен. Корреляцию между величиной делеции хромосомного материала и клиническими симптомами установить весьма трудно. Без своеобразного крика у больного надежный диагноз до цитогенетического исследования установить невозможно, так как большинство клинических симптомов этой болезни встречается и при других хромосомных аномалиях.
Симптомы
Внешние особенности
Короткая шея. Из-за недоразвития шейных позвонков и хрящевой ткани между ними дети не могут повернуть голову под таким же углом, как здоровые люди.
Аномальная форма и расположение глаз отчасти обусловлены неправильным развитием черепных костей. Большая часть этих симптомов характерна также для синдрома Дауна:
— Антимонголоидный разрез глаз. Встречается он не у всех новорожденных. Глазные щели в таком случае идут под небольшим углом, от переносицы вбок и вниз. Внутренний угол расположен выше, чем наружный.
— Косоглазие (страбизм). Характеризуется нарушением симметричности роговиц по отношению к краям и углам век. Ребенку крайне трудно сфокусировать зрение на определенном предмете, и, как правило, зрение у таких детей значительно снижается.
Дефекты развития пальцев:
Синдактилия – сращение пальцев на руках и ногах новорожденного.
Клинодактилия характеризуется искривлением пальцев в суставах.
Косолапость характеризуется сильным отклонением внутрь стопы по отношению к продольной линии голени. У детей с таким дефектом могут быть проблемы с хождением на двух ногах, многие начинают ходить позже сверстников. Данный симптом не является специфическим для синдрома кошачьего крика и может встречаться при других заболеваниях
Кроме того, встречаются:
Генетика
Кариотип 46 XX, 5p- или 46 ХУ, 5р-.
Цитогенетически у всех больных обнаруживается укорочение приблизительно на треть и более короткого плеча одного из гомологов 5-й хромосомы. В коротком плече находится участок (15,1-15,2), который непосредственно вызывает развитие этого синдрома. Кроме обычной делеции, хромосомная перестройка может быть представлена другими вариантами (кольцевая хромосома, транслокация, мозаицизм по делеции).
Особенности строения лица у пациентов с синдромом кошачьего крика в возрасте 8 мес (A), 2 года (B), 4 года (C) и 9 лет (D)
Частота синдрома примерно 1:45000. Соотношение полов М1 : Ж1,3.
Продолжительность жизни у больных значительно снижена, только около 14% из них переживают возраст 10 лет. Но есть и случаи, когда люди с этим синдромом преодолевали порог 50 лет, к примеру, в США известен пациент с синдромом Лежена, которому сейчас 61 год.
Лечение
Лечения нет (паллиативная терапия).
Необходимо постоянное наблюдение со стороны педиатра и психоневролога. Врачами рекомендуются средства, стимулирующие психомоторное развитие ребенка, гимнастика и лечебный массаж
Профилактика
Профилактика заключается в своевременном проведении медико-генетического консультирования в семьях, где имелись больные с синдромом Лежена и основывается на определении кариотипа родителей, у которых был больной ребенок. Наличие изменений короткого плеча 5-й пары хромосом является абсолютным показанием для антенатального определения кариотипа плода при последующих беременностях путем амниоцентеза и исследования амниотических клеток. Сбалансированная транслокация у одного из родителей требует также исследования кариотипа у его кровных родственников с целью выявления лиц, имеющих транслокацию.
Презентацию подготовила
Дякова Мария
Студентка 5 курса,
1 медицинского факультета,
2 группы
БОЛЕЗНЬ КОШАЧЬЕЙ ЦАРАПИНЫ
Несмотря на то что первое клиническое описание болезни кошачьей царапины (БКЦ) было дано R. Debre и соавт. более 50 лет назад, до сих пор вопрос об этиологии этого заболевания остается предметом дискуссий и специальных исследований.
Несмотря на то что первое клиническое описание болезни кошачьей царапины (БКЦ) было дано R. Debre и соавт. более 50 лет назад, до сих пор вопрос об этиологии этого заболевания остается предметом дискуссий и специальных исследований. Поскольку выделить возбудитель от больных не удавалось в течение длительного времени, первоначально предполагалась вирусная или хламидийная этиология заболевания. Первые убедительные сведения об идентификации возбудителя БКЦ были получены только в 1983 г., когда исследователи, используя метод окраски по Warthin-Starry (метод серебрения), обнаружили в ткани пораженных лимфатических узлов у 29 из 34 больных БКЦ мелкие полиморфные грамотрицательные бациллы, которые удалось культивировать лишь в 1988 г. Именно этот микроорганизм первоначально был признан возбудителем БКЦ и получил название Alipia felis.
Тем не менее многочисленные последующие исследования не подтвердили четкой взаимосвязи развития БКЦ с A. felis: в большинстве случаев у больных в пораженных тканях не только не обнаруживался указанный возбудитель, но и в сыворотке крови не выявлялись антитела к нему. Более того, из ткани пораженных лимфоузлов был изолирован еще один возбудитель — Bartonella henselae. Методом ПЦР с применением специфических праймеров к Bartonella spp. и A. felis у больных, у которых кожный тест на БКЦ оказался положительным, было установлено, что в 96% случаев у них обнаруживалась ДНК Bartonella, тогда как ДНК A. felis не выявлялась ни в одном случае (A. Bergmans et al., 1995). Сходные данные, подтверждающие ключевую роль B. henselae в развитии БКЦ, были получены и другими исследователями при использовании непрямой реакции флюоресцирующих антител.
В то же время первоначальный факт обнаружения A. felis в пораженных лимфатических узлах игнорироваться не должен. На сегодняшний день некоторые исследователи допускают, что A. felis способен вызывать заболевание, которое по своей клинической картине может напоминать БКЦ.
Болезнь кошачьей царапины (лимфоретикулез доброкачественный) относится к группе бартонеллезов и характеризуется как нетяжелое самокупирующееся заболевание с развитием одностороннего лимфаденита, регионарного по отношению к месту инокуляции возбудителя, и только в редких случаях возможна диссеминация возбудителя с поражением центральной нервной системы и висцеральных органов.
B. henselae характеризуется как небольшая плеоморфная, грамотрицательная бацилла, весьма требовательная к условиям культивирования (растет только на средах с 5% кровяного агара при температуре от 35 до 37°С, с 5—10% углекислого газа и 40-процентной влажностью). Кроме этого, колонии первичной культуры растут медленно и становятся видимыми только после 9—15 дней роста. При последующем пассаже рост колоний ускоряется. Идентификация выделенного возбудителя проводится с использованием специфических антисывороток, определением профиля жирных кислот клеточной стенки или молекулярно-генетическим методом. С помощью этого метода было идентифицировано два генотипа B. henselae, хотя до сих пор четкой зависимости между генотипами возбудителя и особенностями клинического течения вызываемых ими заболеваний не установлено.
B. henselae на сегодняшний день рассматривается как основной возбудитель БКЦ, однако у 5—15% больных с диагнозом, установленным на основании клинико-эпидемиологических данных, даже с помощью существующих современных методов лабораторной диагностики этиологическое значение B. henselae в развитии заболевания не подтверждается.
Один из необъяснимых парадоксов, связанных с B. henselae: в последние годы установлено, что данный возбудитель ответственен за развитие не только БКЦ, но и некоторых других заболеваний.
БКЦ имеет широкое географическое распространение и встречается практически повсеместно. Основным естественным резервуаром B. henselae являются кошки, инфицированность которых в значительной степени определяет распространенность БКЦ (K. M. Zangwill et al., 1993). По данным некоторых исследователей, у более чем 50% домашних и диких кошек обнаруживается бактериемия, обусловленная B. henselae. В ходе исследования, проведенного в США, установлено, что наиболее высокий процент инфицированности кошек и, соответственно, заболеваемости БКЦ среди людей регистрируется в южных штатах. Большинство исследователей подчеркивают особую роль котят в передаче возбудителя, указывая, что у взрослых кошек редко выявляется бактериемия B. henselae за счет наличия у них специфических антител, свидетельствующих о длительности их инфицирования. Особенностью течения бартонеллеза у кошек является его продолжительность (месяцы, годы) и бессимптомность (даже в случае подтверждаемой бактериемии).
В циркуляции B. henselae среди кошек исключительную роль играют блохи (Ctenocephalides felis). Экспериментальным путем было установлено, что при отсутствии блох инфицирования здоровых кошек не происходит.
B. henselae обнаруживается в кишечнике блох и их испражнениях в течение 9 дней после инфицирования, что свидетельствует о его репликации и персистенции в организме блох. Кроме этого, экспериментально была установлена возможность инфицирования кошек путем внутрикожной инокуляции инфицированных испражнений блох, в то же время оральное введение кошкам инфицированных блох и их испражнений к сероконверсии не приводило. Роль блох в передаче возбудителя от кошек к человеку в настоящее время категорически не отрицается. В последние годы исследователями в США и Италии (Y. O. Sanogo et al., 2003) молекулярно-генетическими методами было продемонстрировано, что ДНК B. henselae может обнаруживаться в иксодовых клещах, хотя их роль в качестве вектора передачи возбудителя БКЦ по-прежнему не изучена.
«Травматический» контакт с кошками (царапины, укусы) весьма характерен для БКЦ и отмечается более чем у 90% заболевших. Установлено, что «резервуаром» B. henselae могут быть и собаки, однако достоверно подтвержденных случаев заражения от них людей пока не описано.
Эпидемиологические исследования показывают, что в сыворотке крови около 20% владельцев кошек и 3–4% общей популяции людей обнаруживаются антитела к B. henselae. Семейные случаи заболевания БКЦ не столь типичны и регистрируются менее чем у 5% пациентов. Хотя БКЦ может развиваться в любом возрасте, чаще заболевают молодые люди (до 18 лет).
Передача возбудителя БКЦ реализуется главным образом контактным путем через царапины, укусы или слюну инфицированных кошек. Подъем заболеваемости, как правило, отмечается с конца лета, что объясняется особенностями жизненного цикла у кошек и блох.
Поскольку возбудитель БКЦ был идентифицирован относительно недавно, многие аспекты, касающиеся патогенеза заболевания, до сих пор недостаточно изучены. Характер развивающегося инфекционного процесса, обусловленного действием B. henselae, в значительной степени зависит от иммунного статуса человека: в тех случаях, когда заболевание развивается у иммунокомпетентных пациентов, диссеминация возбудителя отсутствует, и процесс преимущественно ограничивается локальными или регионарными поражениями. В частности, БКЦ в большинстве случаев проявляется развитием регионарной лимфаденопатии. Поражение висцеральных органов описано только в отдельных случаях (Dunn et al., 1997), а бактериемия у иммунокомпетентных пациентов регистрируется исключительно редко (Slater et al., 1990). Напротив, у иммунокомпрометированных пациентов для инфекции B. henselae типично развитие бактериемии и других системных поражений, включая бациллярный ангиоматоз и бациллярный пелиозный гепатит, а у лиц с врожденными и приобретенными аномалиями клапанов сердца — эндокардит (Raoult et al., 1996).
Гистологические изменения в пораженных лимфатических узлах характеризуются пролиферацией гистиоцитов и B-лимфоцитов, приводящей к образованию гранулем с последующей нейтрофильной инфильтрацией и развитием центрального или звездчатого некроза.
Хотя B. henselae и считается одним из наиболее вероятных возбудителей БКЦ, тем не менее, согласно современным наблюдениям, данный возбудитель ответственен за развитие ряда других патологических состояний человека (табл. 1). При этом иммунный статус больных рассматривается как ключевой фактор, определяющий характер формирующегося заболевания, хотя известны случаи, когда даже у лиц с ВИЧ-инфекцией в стадии СПИДа БКЦ протекала в типичной форме.
 |
| Таблица 1. Заболевания человека, вызываемые B. henselae |
Инкубационный период у больных с БКЦ может варьировать в достаточно широких пределах — от 3 до 20 дней и более, составляя в среднем 1–2 нед. Хотя общепринятой клинической классификации БКЦ нет, чаще всего выделяют типичную и атипичные формы заболевания (табл. 2), что определяется по доминирующему в клинической картине болезни синдромокомплексу.
В типичных случаях БКЦ проявляется развитием первичного аффекта и регионарного (к месту входных ворот инфекции) лимфаденита. Локализация первичного аффекта определяется местом первичной инокуляции возбудителя, а именно местом нанесения кошкой царапин и укусов. По истечении нескольких дней (от 3 до 10), когда нанесенные кошкой повреждения кожи уже заживают, в месте входных ворот формируется папула, которая, как правило, трансформируется в везикулу и далее в пустулу, а после вскрытия — в язвочку, покрытую корочкой. В некоторых случаях пустула может подсыхать без образования язвочки. В диаметре размер формирующейся папулы, как правило, составляет от 1–2 до 5 мм. Частота выявления первичного аффекта у больных БКЦ, по данным различных исследователей, может колебаться от 25 до 94%. Кожные проявления сохраняются в течение 1—3 нед и спонтанно разрешаются.
Регионарный лимфаденит является одним из наиболее постоянных и характерных клинических признаков БКЦ (табл. 3) и сохраняется в течение длительного времени: от 7 до 60 дней, а в отдельных случаях до 1 года и даже 3 лет. В большинстве случаев лимфаденит разрешается в течение 1—4 мес. Нередко он оказывается практически единственным проявлением БКЦ. В большинстве случаев (85%) у больных выявляются одиночные лимфатические узлы, реже множественные, в границах одной анатомической области. Несмотря на то что у больных регистрируется увеличение лимфатических узлов, осуществляющих дренаж места первичной инокуляции возбудителя, развитие лимфангоита не характерно для БКЦ. У 1/3 пациентов могут определяться увеличенные лимфатические узлы разных анатомических областей, хотя генерализованная лимфаденопатия встречается достаточно редко. Размером увеличенные лимфатические узлы чаще бывают от 1 до 5 см, в некоторых случаях до 8—10 см. При пальпации лимфатические узлы умеренно болезненные. Хотя они и не спаяны с окружающими тканями, нередко определяется гиперемия кожных покровов над ними. В 10—50% случаев у больных БКЦ развивается нагноение пораженных лимфатических узлов с образованием густого желто-зеленого гноя. В отдельных случаях при посеве гноя на питательные среды удается получить рост стафилококков и другой флоры, хотя роль условно-патогенной флоры (суперинфекция) в нагноении пораженных лимфатических узлов пока не установлена.
Общее состояние больных в большинстве случаев остается удовлетворительным. Только в трети случаев у больных отмечается повышение температуры тела свыше 38,3°С, которое сохраняется около недели и лишь иногда может затягиваться до месяца и более. Среди других клинических проявлений БКЦ могут отмечаться: слабость и недомогание (30%), головная боль (14%), тошнота и рвота (15%), спленомегалия (11%). В случае длительного течения заболевания у больных может наблюдаться потеря веса. Нередко заболевание приобретает волнообразное течение.
Поражение глаз (глазной вариант) при БКЦ регистрируется в том случае, когда местом инокуляции возбудителя служит слизистая оболочка глаз. Клинические проявления заболевания в этом случае будут включать развитие одностороннего поражения в виде язвенно-гранулематозного конъюнктивита, отека век и преаурикулярной лимфаденопатии (синдром Парино). Одновременно у больных могут определяться умеренно увеличенные и болезненные околоушные и шейные лимфатические узлы. К числу других глазных проявлений БКЦ относятся нейроретинит, неврит зрительного нерва и папиллит. Для нейроретинита типично одностороннее острое нарушение остроты зрения, развивающееся на фоне умеренно выраженных явлений интоксикации. При осмотре глазного дна могут выявляться геморрагии, множественные дискретные повреждения, ватоподобные образования, отек и экссудация соска зрительного нерва (симптом «макулярной звезды») (J. B. Reed et al., 1998).
Поражение нервной системы (неврологический вариант) у больных БКЦ выявляется редко (
2% случаев), хотя диапазон клинических проявлений весьма разнообразен: у больных могут выявляться радикулиты, полиневриты, миелит, энцефалопатия, энцефалит, менингит и церебральная атаксия. Характерным признаком поражения нервной системы при БКЦ является то, что они развиваются спустя 1—6 нед (чаще 2–3 нед) от момента появления лимфаденопатии. Для развития энцефалита и менингита типично внезапно возникающее ухудшение состояния больного, сопровождающееся лихорадкой, головной болью, спутанностью сознания и дезориентацией. В некоторых случаях состояние может прогрессивно ухудшаться, вплоть до развития комы. В ликворе у таких больных определяется мононуклеарный плеоцитоз. Только в отдельных случаях у больных после перенесенного энцефалита могут отмечаться резидуальные явления.
Некоторые авторы (P. M. Delahoussaye, B. M. Osborne, 1990), указывая на возможность поражения печени и селезенки при БКЦ, выделяют висцеральный вариант заболевания, для которого характерны длительная волнообразная лихорадка, увеличение размеров печени и селезенки, повышение в сыворотке крови уровней аминотрансфераз, с определением при УЗИ и компьютерной томографии множественных, диффузных, гипоэхогенных дефектов. Довольно часто у таких больных отмечается генерализованная лимфаденопатия.
Кроме этого, в более редких случаях у больных БКЦ могут выявляться абсцесс селезенки, плеврит, эндокардит, пневмония, узловатая эритема, тромбоцитопеническая пурпура, остеомиелит (B. Dzelalija et al., 2001, C. V. Hulzebos et al., 1999).
В типичных случаях первичная диагностика БКЦ не представляет больших сложностей, поскольку основывается на характерных клинико-эпидемиологических данных (табл. 4).
Определенные сложности имеются при лабораторной верификации диагноза, что связано с отсутствием соответствующей лабораторной базы. В зарубежной практике длительное время в качестве основного диагностического критерия БКЦ использовался кожный тест, в котором в качестве аллергена применялся термоинактивированный пунктат, полученный из лимфоузлов больных с установленным (в соответствии с принятыми критериями) диагнозом БКЦ. По данным многих авторов, результативность такого теста достигала 95—98%, однако из-за риска передачи гемоконтактных инфекций использование данного теста ограничено, а кожного теста с использованием очищенных антигенов B. henselae пока не описано.
Микробиологические исследования в широкой практике не применяются ввиду длительности (от 2 до 6 нед) и сложности проведения анализа.
Достаточно информативным способом установления диагноза является биопсия папул и/или пораженных лимфатических узлов с последующим гистологическим исследованием (окрашивание срезов гематоксилин-эозином и серебром — метод Warthin-Starry), позволяющим выявить характерные гистологические признаки поражения и скопление мелких плеоморфных бактерий.
В последние годы большое внимание уделяется разработке специфических иммунологических (ИФА) и молекулярно-генетических (идентификация гена 16S рибосомальной РНК B. henselae) методов обнаружения возбудителя БКЦ в биопсийном материале больного, хотя пока для широкой практики они по-прежнему недоступны.
Дифференциальный диагноз необходимо проводить с заболеваниями, сопровождающимися развитием лимфаденопатии (табл. 5).
Несмотря на то что в редких случаях отмечаются варианты тяжелого течения БКЦ, у иммунокомпетентных лиц прогноз заболевания благоприятный. Повторных случаев и летальных исходов не описано.
Многочисленные клинические наблюдения показывают, что в большинстве случаев БКЦ протекает как самокупирующаяся инфекция, и применение антибактериальной терапии не оказывает существенного влияния на ее течение. Традиционные рекомендации по применению эритромицина (эритромицин-тева, зинерит) и доксициклина (юнидокс солютаб, медомицин, вибрамицин, тетрадокс) основаны на эффективности этих препаратов у больных с ВИЧ-инфекцией при развитии бациллярного ангиоматоза, вызываемого Bartonella quintana, тогда как у больных БКЦ терапевтическая эффективность указанных препаратов не подтверждена ни в одном исследовании. Весьма противоречивыми остаются данные по соответствию чувствительности in vitro возбудителя БКЦ к антибактериальным препаратам и их клинической эффективности. Единственным антибактериальным препаратом, клиническая эффективность которого была установлена в ходе рандомизированного плацебо-контролируемого исследования, является азитромицин (сумамед, хемомицин, азивок, сумазид), назначаемый в течение 5—10 дней. В неконтролируемых исследованиях (A. M. Margileth, 1992) из 18 антимикробных препаратов клиническая эффективность была установлена только при применении рифампицина (бенемицин, р-цин), ципрофлоксацина (ципросан, цифран, ципрова), гентамицина (гентамицин К, гентамицина сульфат) и триметопримсульфаметоксазола (бактрим, септрин). Антибактериальные препараты при БКЦ следует применять у иммунокомпрометированных лиц и при тяжелом течении заболевания, сопровождающегося поражением нервной системы и висцеральных органов.
В случае выявления флуктуации в пораженном лимфатическом узле требуется его пункция и аспирация гноя, что ускоряет последующий процесс склерозирования и рубцевания ткани лимфатического узла и влияет в конечном итоге на выздоровление пациента.
По вопросам литературы обращайтесь в редакцию.
В. А. Малов, доктор медицинских наук, профессор
А. Н. Горобченко, кандидат медицинских наук, доцент
ММА им. И. М. Сеченова, Москва