Костный остаток
«. Костный остаток: пищевой продукт убоя в виде костной массы, полученной после механической дообвалки кости на прессах различных конструкций. «
Источник:
«ПРОМЫШЛЕННОСТЬ МЯСНАЯ. ПРОДУКТЫ ПИЩЕВЫЕ. ТЕРМИНЫ И ОПРЕДЕЛЕНИЯ. ГОСТ Р 52427-2005»
(утв. Приказом Ростехрегулирования от 28.12.2005 N 380-ст)
Смотреть что такое «Костный остаток» в других словарях:
костный остаток — Пищевой продукт убоя в виде костной массы, полученной после механической дообвалки кости на прессах различных конструкций. [ГОСТ Р 52427 2005] Тематики производство мясных продуктов … Справочник технического переводчика
КРОВЬ — КРОВЬ, жидкость, заполняющая артерии, вены и капиляры организма и состоящая из прозрачной бледножелтоват. цвета плаз мы и взвешенных в ней форменных элементов: красных кровяных телец, или эритроцитов, белых, или лейкоцитов, и кровяных бляшек, или … Большая медицинская энциклопедия
Кость — У этого термина существуют и другие значения, см. Кость (значения). У этого термина существуют и другие значения, см. Кости (значения). Кость, как орган живого организма, сос … Википедия
Кости — твердые части, соединение которых составляет скелет или остов тела позвоночных и которые характеризуются большой твердостью, значительным содержанием минеральных веществ и своеобразным микроскопическим строением (см. ниже). В состав К. входят как … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Характеристики — К.4. Характеристики Применяют следующие дополнительные характеристики: К.4.3.1.2. Номинальное напряжение изоляции Минимальное значение номинального напряжения изоляции должно быть 250 В. К.4.3.2.1. Условный тепловой ток на открытом воздухе… … Словарь-справочник терминов нормативно-технической документации
СЕПСИС — (sepsis, septicaemia), общее инфекционное заболевание, определяемое своеобразной реакцией организма на постоянную или периодическую инфекцию крови различными микроорганизмами и их токсинами, не сопровождающуюся какими либо специфическими… … Большая медицинская энциклопедия
Новорождённый — I Новорожденный (neonatus) ребенок с момента рождения до четырехнедельного возраста. Этот период жизни ребенка носит также название неонатального. В зависимости от срока беременности к моменту рождения различают доношенных, недоношенных и… … Медицинская энциклопедия
ОБЛИТЕРАЦИЯ — (лат. obliteratio уничтожение), термин, употребляемый для обозначений закрытия, уничтожения той или иной полости или просвета посредством разрастания^ ткани, идущего со стороны стенок данного полостного образования. Указанное разрастание чаще… … Большая медицинская энциклопедия
После удаления зуба из десны выходят какие-то кусочки
Большинство из нас хоть раз в жизни удаляли зубы. А многие и не раз. Иногда пациенты жалуются, что после удаления из десны еще долго выходят мелкие осколки непонятно чего, то ли зуба, то ли кости. Говорит ли это о плохом качестве удаления или нет?
Вопрос непростой, ситуации бывают самые разные, поэтому попробуем объяснить подробно каждую.
Вариант первый: из лунки выходят осколки удаленного зуба
Если из лунки вылезают действительно остатки зуба, то это не хорошо, конечно. Зуб должен быть удален полностью, и никаких его остатков в лунке быть не должно. В крайне редких случаях, когда речь идет о том, что продолжение удаления будет гораздо опаснее и травматичнее для пациента, чем прекращение операции, бывает, что могут что-то оставить на потом.
Какое бы сложное удаление ни было, врач должен удалить зуб полностью. Бывало, что очень сложный зуб удаляли более двух часов, но в результате все равно удалили целиком.
Вариант два: из лунки торчит кусок кости
Когда зуб удален, а десна после этого оседает, острые края кости могут вылезти наружу. Чаще всего хирурги стараются сгладить всё острое, но кость настолько ценный ресурс, что удалять ее фрагменты без крайней необходимости не принято. Стараются сохранить любой фрагмент кости, чтобы дать возможность лунке лучше зарасти и не дать большую усадку после удаления зуба.
А если экзостоз все же вылез и мешает пациенту, то его вполне можно загладить и позже. Это обычная рутинная процедура.
Вариант три: не зуб и не кость, а костный материал
Если это не зуб и не кость, тогда что? Современные хирурги часто после удаления подкладывают в лунку специальный костный материал для того, чтобы вместо дырки от зуба поскорее образовалась нормальная здоровая кость, куда можно будет впоследствии установить имплантат. Это могут быть так называемые костные чипсы, порошок и т.д.
Крупинки этой искусственной кости иногда тоже могут потихоньку выходить из лунки через шов, а пациент думает, что это выходят кусочки зуба.
Так что далеко не всегда то, что пациент принимает за осколки зуба, этим зубом действительно является, и это никак не говорит о плохой квалификации хирурга.
В любом случае лучше до удаления зубы не доводить!
Специфика костного материала bio oss
Атрофия костной ткани – это уменьшение объема челюстной кости, которая развивается на фоне отсутствия моляров и премоляров в течение продолжительного периода времени. Обнаружить его удается только при посещении стоматологического кабинета. Это связано с тем, что визуально человеку может быть незаметна атрофия.
Чаще всего с целью восстановления костной ткани прибегают к помощи биоматериала Bio-Oss. Он пользуется особым спросом, за годы применения был накоплен большой опыт по его использованию. Он имеет природное происхождение, за счет чего химически и структурно совместим с минерализованной костью человека. В ходе ряда клинических исследований была подтверждена безопасность и надежность материалов. Рассмотрим подробнее, какими преимуществами он обладает, и в каких ситуациях применяют.
Причины потери костной ткани
Убыль костной ткани способна развиться на фоне одного или нескольких факторов. Основная причина появления недуга – утрата зубов. Спустя 4-6 месяцев после их удаления, челюстная кость начинает существенно сокращаться в объеме, а через 12 месяцев доходит до своего минимума. Среди других факторов, провоцирующих атрофию костной ткани, отмечают:
Когда необходимо восстанавливать кость?
Восстановление необходимо при пародонтите, чтобы сохранить здоровые зубы, которые потеряли связь с костью. Часто врачи проводят увеличение объема костной ткани, если ее недостаточно для осуществления надежной имплантации. Во время осуществления операции синус-лифтинг восстановление требуется для замещения недостающей кости в верхнечелюстных пазухах. Во время цистэктомии восстановление необходимо для замещения приобретенного дефекта.
Характеристики костного биоматериала Bio-Oss
Костнозамещающий материал bio oss производит ведущая компания Geistlich Pharma. Она признана одним из крупнейших производителей биоматериалов для регенерации костной и мягких тканей. Страна-производитель: Швейцария. В процессе производства предусмотрена высокая степень очистки с соблюдением строгих правил техники безопасности. Производство включает стерилизацию одних продуктов сухим жаром, а других – облучением γ-лучами.
Bio-Oss состоит из крупного рогатого скота – бычьей кости. По своей структуре бычья кость является практически идентичной структуре человеческой кости. Это гарантирует быструю адгезию клеток: обеспечивается их ускоренное сцепление и регенерация тканей. Кроме того предоставляется костная матрица для прорастания новой ткани.
Благодаря высокопористой микроструктуре, натуральный костный материал способен обеспечивать беспрепятственный ангиогенез и остеогенез, сохраняя при этом объем на протяжении длительного периода времени. Bio-Oss характеризуется шероховатой поверхностью, способствующей прикреплению и размножению костных клеток.
Средство отличается широким ассортиментом. Для удобства его выпускают в разных формах – в виде блока, гранул, коллагеновой мембраны или матрицы. Принцип действия Био-Осс состоит в том, что материал заполняет образовавшиеся пустоты в костной ткани, создавая некий каркас и естественную среду для восстановления кровеносных сосудов в поврежденной области кости.
Существует и другой достойный материал – Био-Гайд (Gide) с натуральной белковой структурой. Он представляет собой резорбируемую мембрану, которая не дает врастись мягкой ткани в область дефекта, гарантируя быстрое заживление раны. Ее применение способствует достойному результату процедур по восстановлению костной ткани и имплантации моляров и премоляров.
Основные преимущества
Костный материал bio oss успешно применяют ведущие врачи-стоматологи уже долгие годы, в частности, специалисты клиники «А-Медик». К его достоинствам относятся:
Основные показания и противопоказания к применению
Био осс (костный материал) характеризуется широким спектром показаний для применения в различных сферах, в частности, челюстно-лицевой хирургии, хирургической стоматологии и имплантологии. Его используют для заполнения лунки зуба после удаления, чтобы сохранить объем кости для дальнейшей имплантации. Зачастую к помощи bio oss прибегают при выполнении операции синус-лифтинга. При выполнении одномоментной имплантации проводят заполнение зазоров после установки имплантата.
Также, материал необходим для оптимальной стабильности объема в области выраженных дефектов и проведении операции вертикальной и горизонтальной аугментации (заполнения зазоров после фиксации блока и нанесение прослойки гранул, чтобы значительно улучшить контур аугментата). Иногда требуе6тся заполнение дефектов кости после проведения цистэктомии (хирургической операции по удалению кисты зуба вместе с поврежденной частью корня).
Гранулы выпускают разных размеров, что определяет их основное назначение. Гранулы размера «S» требуются для заполнения небольших костных дефектов, зазоров между блоком и костью, поскольку они лучше адаптируются к поверхности. Гранулы размера «L» требуются для проведения операций синус-лифтинга и серьезных дефектов.
Однако, несмотря на ряд преимуществ и широкого спектра показаний, к применению материала bio oss существует ряд противопоказаний. К ним относятся:
Особенности оперативного вмешательства
Как правило, восстановление кости и установку имплантата осуществляют одновременно. Для формирования новой кости дефект заполняют биоматериалом Био-Осс, а для направленной регенерации на рану накладывают мембрану Био-Гайд.
После проведения оперативного вмешательства возможно появление небольшой припухлости и отечности, которые можно устранить с помощью холодного компресса. Первые 10-14 дней во время чистки зубов следует избегать травм оперированного участка, пользоваться антибактериальным ополаскивателем. При появлении сильных болезненных ощущениях врач может назначить обезболивающее средство. При этом важно регулярно показываться врачу-стоматологу даже в том случае, если ничего не беспокоит и заживление протекает благополучно.
Костный материал bio oss: отзывы
Александр, 30 лет. Потерял два зуба несколько лет назад, долго не ходил к врачам и никак не решал эту проблему. Недавно понадобилась помощь стоматолога, записался на прием в клинику «А-Медик». Очень понравилось чуткое отношение врача! Провел диагностику и посоветовал провести имплантацию. Во время нее специалист использовал материал Био-Осс, чтобы восстановить утраченную костную ткань. Процедура прошла хорошо, побочная реакция на материал не возникла.
Оксана, 43 года. В прошлом месяце в клинике «А-Медик» мне проводили синус-лифтинг с применением швейцарского материала Bio-Oss. Заранее прочитал о нем отзывы в интернете, все писали, что материал достойный. Теперь я полностью с ними согласен!
Современные подходы к диагностике и лечению остеопороза
Рисунок 1. Микроархитектоника здоровой (слева) и остеопоретической (справа) трабекулярной кости. Методы диагностики остеопороза Денситометрия. Ультразвуковая сонография. Рентгенография. Исследование биохимических маркеров костного метаболи
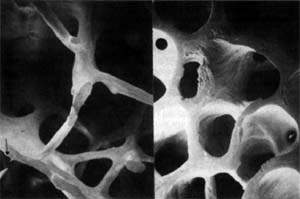 |
| Рисунок 1. Микроархитектоника здоровой (слева) и остеопоретической (справа) трабекулярной кости. |
Методы диагностики остеопороза Денситометрия. Ультразвуковая сонография. Рентгенография. Исследование биохимических маркеров костного метаболизма.
Остеопороз — это системное заболевание скелета, характеризующееся снижением костной массы и нарушением микроархитектоники костной ткани, ведущими к повышенной хрупкости костей с последующим увеличением риска их переломов (рис. 1). Помимо наиболее распространенного постменопаузального остеопороза, в настоящее время в цивилизованных странах в связи с растущей продолжительностью жизни все чаще встречается сенильный остеопороз, а также вторичный остеопороз, обусловленный различными заболеваниями (эндокринная патология, ревматические болезни, заболевания желудочно-кишечного тракта и пр.) или связанный с длительным приемом некоторых лекарственных препаратов, например кортикостероидов.
В настоящее время для диагностики остеопороза используются преимущественно неинвазивные методы, которые легковыполнимы, безопасны и могут повторяться неоднократно у одного и того же больного. К таким методам относятся рентгенографическое исследование, костная денситометрия и исследование биохимических маркеров костного метаболизма. Каждый из этих методов занимает свою нишу в диагностике заболе-вания.
С целью ранней диагностики остеопороза применяются различные технологии, объединенные под общим названием «костная денситометрия», с ее помощью можно определить минимальную плотность костной ткани (МПК), являющуюся главным критерием прочности кости. В настоящее время выделяют четыре типа и два подтипа технологий для измерения МПК:
В данном перечне отсутствует фотонная денситометрия — предшественница рентгеновской денситометрии, в последнее время используемая весьма редко.
 |
| Рисунок 2 |
Системы DXA являются наиболее изученными и широко применяются в клинической практике (рис. 2). DXA позволяет измерять МПК в центральных отделах скелета: в поясничном отделе позвоночника и в проксимальном отделе бедренной кости. В этих участках происходят наиболее тяжелые переломы. Кроме того, многие из этих приборов снабжены программой «все тело», позволяющей определить содержание минералов во всем скелете, а также исследовать мягкие ткани — мышечную и жировую. В новых модификациях приборов DXA имеется возможность латерального сканирования и морфометрического измерения позвонков,что значительно повышает информативность этого метода. Метод DXA также адаптирован для оценки состояния МПК в области периферических участков скелета, в частности в области предплечья и пяточной кости (рис. 3).
Радиографическая абсорбциометрия используется редко, поскольку требует специально оборудованного центра, где при помощи микроденситометра производится сканирование рентгеновских снимков фаланг и определяется их оптическая плотность.
 |
| Рисунок 3 |
Для определения МПК позвоночника можно использовать и QCT, которая является единственным методом, представляющим результаты исследования в трехмерном измерении. Возможность проведения измерений в поперечном сечении, заложенная в QCT, позволяет выделить этот метод среди других, так как он дает возможность дифференцированно оценивать МПК в трабекулярной и кортикальной костной ткани, фиксируя истинные значения МПК в г/см3 [1]. В отличие от DXA при QCT нет искажений МПК, связанных с тучностью пациента, а также вызванных сопутствующей патологией, например спондилоартритом и остеофитами, обызвествлением стенки аорты или участками остеосклероза, развивающимися в результате дегенеративных заболеваний или переломов позвонков. Но большие дозы облучения при QCT, а также высокая стоимость обследования ограничивают широкое применение этой технологии в диагностике остеопороза, использование ее оправданно лишь в ситуациях, требующих дифференциальной диагностики (рис. 4).
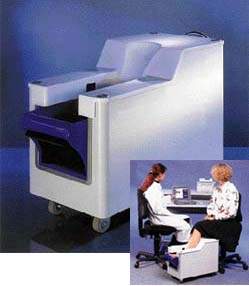 |
| Рисунок 4 |
В последние годы активно развивается ультразвуковая сонография, которая, в отличие от рентгеновской денситометрии, позволяет обследовать другие характеристики костной ткани: SOS — скорость распространения ультразвука в кости и BUA — широковолновое рассеивание (затухание) ультразвуковой волны в исследуемом участке скелета. Эти параметры, по данным многих исследователей, отражают степень эластичности и прочности костной ткани и достаточно высоко коррелируют с МПК позвоночника и шейки бедра [2]. В настоящее время многие специалисты высказывают мнение о том, что с помощью ультразвуковой денситометрии можно предсказывать риск переломов, тем самым обосновывая ее значение как метода для скрининга. Вопрос о возможности применения этих приборов в диагностике остеопороза и оценке эффективности терапии продолжает дискутироваться.
Рентгенография довольно активно используется для диагностики остеопороза и его осложнений. Однако ее нельзя отнести к методам ранней диагностики, поскольку рентгенологические признаки остеопороза появляются тогда, когда 20 — 30% костной массы уже потеряно [3]. Наиболее сложно оценить выраженность остеопороза в позвоночнике, поскольку ни один из его рентгенологических признаков не является специфичным. Часто рентгенография позволяет выявить остеопороз лишь на поздней стадии, когда уже имеются остеопоретические переломы. Для объективной оценки степени снижения минерализации костей разработаны так называемые полуколичественные методы. В основе их лежит вычисление вертебральных, феморальных и метакарпальных индексов. Но они также не могут претендовать на достаточную точность и чувствительность при выявлении ранней стадии заболевания (остеопении), хотя успешно применяются при эпидемиологических исследованиях распространенности остеопороза в популяции [4, 5]. Таким образом, основной функцией ренгенографического метода в диагностике остеопороза является обнаружение переломов, динамическое наблюдение за появлением новых переломов и дифференциальная диагностика остеопоретических переломов от других типов деформаций позвоночника.
С помощью методов «костной денситометрии» можно судить об основных параметрах прочности костной ткани, однако эти методы не дают никакой информации об уровне костного метаболизма. Уровень формирования и резорбции костной ткани может быть оценен несколькими способами: путем измерения ферментной активности костных клеток (остеобластов и остеокластов) или определения продуктов деградации костного матрикса, которые высвобождаются в циркуляцию в процессе костного обмена (табл. 1).
Таблица 1. Биохимические маркеры костного метаболизма
маркеры
мочи
Представленные в таблице костные маркеры являются предикторами потери костной массы, переломов костей скелета и используются для мониторинга антиостеопоретической терапии. По этим биохимическим показателям можно судить об эффективности терапии, об адекватности дозы препарата и о его переносимости. Особенно полезны костные маркеры для оценки эффективности терапии в сравнительно короткие промежутки времени, когда денситометрическое исследование еще не информативно (полагают, что повторные денситометрические исследования надо выполнять не чаще одного раза в год). Уровень маркеров костного метаболизма изучался в основном у женщин постменопаузального периода. Оказалось, что уровень почти всех маркеров, за исключением IPCP, повышен и коррелирует со снижением МПК [6]. Полагают, что сочетание денситометрии и исследования биохимических маркеров костного метаболизма позволит получить более полную информацию о риске развития постменопаузального остеопороза. По мнению P. Delmas (1996) увеличение скорости костной резорбции (по оценке уровней биохимических маркеров) существенно повышает риск развития переломов независимо от исходной костной массы пациентов [7]. Это связано с тем, что хрупкость кости при остеопорозе зависит не только от МПК, но и от нарушения микроархитектоники костной ткани, выраженность которой можно оценить с помощью биохимических маркеров костной резорбции. Это предположение подтверждается данными P. Garnero et al. (1996), полученными в рамках исследования EPIDOS [6]. Доказано, что увеличение уровня СТх или свободного диоксипиридинолина на 1SD от нормы ассоциировалось с 1,3- и 1,4-кратным увеличением риска переломов шейки бедра (рис. 5).
 |
| Рисунок 5. Комбинированная оценка МПК и скрытой костной резорбции для определения риска перелома шейки бедра у пожилых. МПК определялась по критериям ВОЗ с учетом показателей ниже 2,5 SD от нормальных показателей МПК у молодых здоровых женщин (Ts core |
При этом снижение МПК шейки бедра и увеличение маркеров костной резорбции, независимо друг от друга, связаны с высоким риском переломов шейки бедра. Для оценки эффективности проводимой терапии рекомендуется исследовать биохимические маркеры через каждые три месяца после начала лечения. При исследовании биохимических маркеров необходимо принимать во внимание факторы, влияющие на воспроизводимость результатов: диета, условия хранения материала, биологические факторы (циркадные и сезонные колебания, менструальный цикл, возраст, пол, наличие сопутствующих заболеваний и т. д.).
Многолетний опыт изучения остеопороза за рубежом показывает, что ни один из существующих в настоящее время лекарственных препаратов не может надежно восстановить количество и качество кости, поэтому основной мерой в борьбе с этим заболеванием является профилактика. Профилактику остеопороза надо начинать рано и уделять особое внимание средовым факторам, влияющим на достижение пика костной массы, который наступает примерно к тридцати годам. В числе этих факторов — питание и физическая активность, адекватное поступление в организм витамина D и инсоляция. К наиболее важным периодам относятся период роста кости (юношество), беременность, лактация и перименопауза. Пик костной массы может быть значительно улучшен за счет включения в рацион продуктов с повышенным содержанием кальция (прежде всего молочные и рыбные продукты). Суточное потребление кальция должно составлять в среднем 1000 — 1500 мг, предпочтительно с пищей. Регулярные физические упражнения с весовой нагрузкой в период роста кости приводят к увеличению пика костной массы. У взрослых после достижения пика костной массы адекватное потребление кальция, постоянная физическая нагрузка и наличие регулярного менструального цикла также способствует сохранению костной массы. Профилактику остеопороза среди взрослого населения нужно проводить в «группах риска».
Проблема лечения остеопороза за рубежом изучается давно, причем особенно активно в последнее десятилетие, что связано с введением денситометрии. Однако до настоящего времени не разработаны общепринятые терапевтические программы и режимы лечения этого заболевания, что, по-видимому объясняется его многофакторной природой и сложным патогенезом. Основная цель лечебных мероприятий — сбалансирование процессов костного метаболизма и сохранение или улучшение качества жизни пациента. Для этого необходимо добиться замедления или прекращения потери костной массы; уменьшить болевой синдром в позвоночнике и периферических костях; улучшить функциональное состояние больного и предотвратить возможные падения; восстановить трудоспособность и психоэмоциональное состояние. Наряду с этиопатогенетической терапией препаратами, направленными на нормализацию процессов ремоделирования костной ткани и на сохранение минерального гомеостаза, применяется и симптоматическая терапия, включающая в себя диету с повышенным содержанием солей кальция и фосфора, нестероидные противовоспалительные средства, анальгетики, миорелаксанты, которые позволяют уменьшить болевой синдром, мышечное напряжение и тем самым расширить двигательную активность пациента и ускорить начало реабилитационных мероприятий.
Реабилитация подразумевает лечебную физкультуру, ношение корсетов, плавание, курсы легкого массажа.
Все препараты для лечения остеопороза можно разделить на три группы:
В этиопатогенетической терапии остеопороза предпочтение отдается группе препаратов, подавляющих резорбцию костной ткани, вследствие их более высокой эффективности и сравнительно небольшого побочного действия.
В целом терапия остеопороза должна быть комплексной и проводить ее следует длительно в виде непрерывного или курсового лечения. Поскольку в настоящее время нет идеального препарата для лечения остеопороза, перспективна комбинированная терапия, в которой сочетаются препараты с различным механизмом действия, что позволяет потенцировать их антиостеопоретическое действие, снизить частоту и выраженность побочных эффектов.
| Профилактика остеопороза заключается в сбалансированном питании, физической активности, и адекватном поступлении в организм витамина D |
При комбинированной терапии лекарственные средства назначают одновременно или последовательно. Их выбор осуществляется индивидуально для каждого больного в зависимости от формы остеопороза, скорости костного обмена, тяжести клинического течения, сопутствующих заболеваний. Основным критерием эффективности любого антиостеопоретического средства является снижение частоты переломов, однако в каждом конкретном случае надо ориентироваться в первую очередь на показатели МПК по данным костной денситометрии и на биохимические маркеры костного обмена. Увеличение МПК более чем на 1% и нормализация биохимических показателей, если они были изменены, свидетельствуют об эффективности проводимой терапии. Учитываться должна и положительная динамика клинической картины: уменьшение болевого синдрома, повышение функциональной активности.
Таким образом, в настоящее время имеется довольно большой выбор диагностических методов, позволяющих установить диагноз остеопороза на разных стадиях, а также эффективных лекарственных препаратов, влияющих на различные звенья патогенеза остеопороза, способных уменьшить или купировать клинически выраженные симптомы заболевания, а также предупредить развитие переломов.





