Лапароскопическая транспозиция яичников что это
Транспозиция яичников за пределы локализации фокуса лучевой терапии, помогает сохранить функции яичников у большинства женщин. Транспозиция яичников уменьшала лучевую нагрузку на каждый по сравнению с яичниками, оставшимися в их обычной локализации. Смещенные яичники получили радиацию в дозе 126 сГр при внутриполостном облучении, от 135 до 90 сГр — при внешнем облучении с общей дозой лучевой терапии 4500 сГр, от 230 до 310 сГр рассеянного облучения — при лучевой терапии на парааортальные узлы с общей дозой 4500 сГр.
Латеральная транспозиция яичника в сравнении с медиальной. Латеральная транспозиция более эффективна, чем медиальная.
В одном исследовании было проведено сравнение 7 больных раком шейки матки, которым проводили латеральную транспозицию яичников, и 9 пациенток с болезнью Ходжкина, которым выполняли медиальную транспозицию. Все они подверглись лучевой терапии. У 6 женщин из 7 с латеральной транспозицией яичников, вынесенных за пределы поля облучения, при КТ выяснилось, что все функции яичников сохранены. Рассеянные дозы облучения, полученные яичниками, составили от 100 до 300 сГр. У одной пациентки, у которой яичники оставались в поле облучения и получили дозу 450 сГр, наступило преждевременное истощение яичников.
После медиальной транспозиции КТ показала, что только 3 из 13 яичников оказались вне поля облучения. Но и на эти 3 яичника вне поля облучения пришлась доза радиации около 300 сГр.
Латеральная транспозиция яичников
Транспозицию яичников можно выполнять разными способами — с помощью лапаротомии или лапароскопии. Если лапаротомия необходима при лечении рака шейки матки с радикальной экстирпацией или требуется определить стадию болезни Ходжкина, одновременно с этим можно выполнить латеральную транспозицию яичников. Однако диагностическая лапаротомия и спле-нэктомия уже не являются необходимыми при I и II стадиях болезни Ходжкина. В случаях, при которых нет необходимости в проведении лапаротомии или транспозиция не была проведена при первой лапаротомии, ее можно выполнить лапароскопическим доступом.
Лапароскопия при транспозиции яичников имеет ряд преимуществ, в результате этот подход стали применять чаще других. Лапароскопическая транспозиция может быть проведена как амбулаторная процедура с незначительным нарушением запланированного графика лечения. Простота выполнения вмешательства позволяет не производить ненужной транспозиции яичников в большинстве случаев рака шейки матки, когда в лучевой терапии нет необходимости. Важное преимущество лапароскопической транспозиции яичников состоит в том, что лучевую терапию можно начать сразу после операции, что предотвращает возвращение яичников в поле облучения.
В случаях рака влагалища или шейки матки, когда лечение проводят с помощью брахитерапии (близкофокусной лучевой терапии), лапароскопическая транспозиция может быть выполнена под той же анестезией, которую используют при введении брахитерапевтического устройства.
Перед хирургическим вмешательством следует обсудить с онкологом, на какое расстояние будут сдвинуты яичники за пределы поля облучения. К примеру, в случае рака прямой кишки обычно зона облучения у пациентки доходит до крестцового мыса. Онкологи часто требуют сдвинуть яичники выше передней ости подвздошной кости. Глубокое паховое кольцо, куда входит круглая связка, направляясь через паховый канал, расположено в середине между лобковым бугорком и передневерхней остью подвздошной кости и хорошо визуализируется при лапароскопии. Обычно яичники сдвигают в эту область. Доза облучения, которая окажет воздействие на яичники, может быть рассчитана после операции.
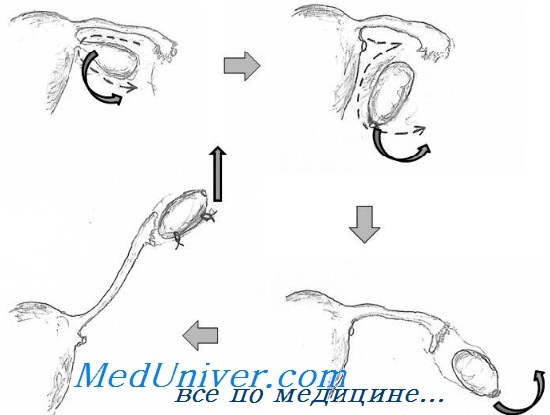
Техника латеральной транспозиции яичников. Существуют различные техники, в зависимости от того, какая нужна мобилизация яичников и собирается ли хирург пересекать маточную трубу. Пересечение маточной трубы позволяет сдвинуть освобожденные придатки, не рассекая брыжейку яичника, в которой располагается анастомоз между кровеносными сосудами, подходящими к трубе и яичнику.
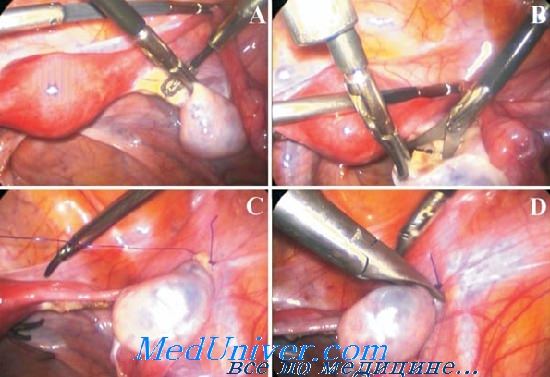
Хирургическое вмешательство начинают с рассечения маточно-яичниковой связки и фаллопиевой трубы. Придатки мобилизуют вместе с сосудами и сдвигают в латеральные каналы. В идеале сосудистая ножка располагается ретроперитонеально и избегает вытягивания, перекручивания или травмы, в то время как у яичников, оставленных интраперитонеально, истончается оболочка. Затем яичник подшивают нерассасывающимися швами к задней стенке абдоминальной брюшины. Клипсы располагают так, чтобы онколог мог определить, где локализуются яичники.
Есть сообщения и о другой технике транспозиции яичников, которая предусматривает меньшую мобилизацию. После рассечения маточно-яичниковой связки яичник не отделяют от фаллопиевой трубы и сосудов, а все вместе мобилизуют. Хотя эта техника была описана в случаях наблюдения, результатом которых была спонтанная беременность, она может не позволять достаточно сдвигать яичники за пределы поля облучения в большинстве случаев онкологических заболеваний, требующих облучения тазовых органов, если цель — облучение участков, расположенных рядом с фаллопиевой трубой. Вряд ли маточная труба способна вытягиваться до передневерхней ости подвздошной кости.
Высокая мобилизация яичника без фаллопиевой трубы была предложена Morice и соавт.. По этой методике маточную трубу не отделяют от матки, но отсепаровывают от яичника. Яичник выделяют, и сосуды яичника пересекают по направлению к бифуркации аорты. Затем ножку поворачивают и прикрепляют к околокишечной складке.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Материалы конгрессов и конференций
VIII РОССИЙСКИЙ ОНКОЛОГИЧЕСКИЙ КОНГРЕСС
ЛАПАРОСКОПИЧЕСКАЯ ХИРУРГИЯ В ОНКОГИНЕКОЛОГИИ
Л.В. Адамян, А.В. Козаченко
ГУ НЦ АГиП РАМН, Москва
За последние два десятилетия в практику оперативной гинекологии широко внедрилась эндоскопическая хирургия. Развитие этой методики позволяет в настоящее время выполнять практически любую гинекологическую операцию по поводу доброкачественной патологии внутренних гениталий путем лапароскопического вмешательства.
Несмотря на то, что впервые эндоскопическую операцию по стадированию рака путем изучения состояния тазовых лимфатических узлов выполнил во Франции в 1986 г. D. Dargent, до сегодняшнего дня лапароскопическая хирургия не нашла широкого применения в онкологии. Использование лапароскопической хирургии в онкогинекологии ограничено в связи с вероятным увеличением риска диссеминации опухолевого процесса. Действительно, при несоблюдении правил абластики в ходе выполнения лапароскопической операции возникают метастазы в передней брюшной стенке в местах введения троакаров при раке яичника и аденокарциноме шейки матки (G. Lane). Кроме того, применение при наложении пневмоперитонеума углекислого газа также может способствовать рассеиванию раковых клеток.
Внедрение в клиническую практику малоинвазивной эндоскопической техники способствует более раннему выявлению злокачественного заболевания, точному установлению стадии его развития (и, соответственно, проведению адекватного лечения), дает возможность выполнять радикальное или паллиативное (в том числе и циторедуктивное) хирургическое вмешательство с более быстрым послеоперационным восстановлением, что способствует раннему началу химиолучевого воздействия, а также позволяет проводить мониторинг за эффективностью проводимого лечения.
Лапароскопический доступ имеет целый ряд существенных преимуществ перед традиционным: он обеспечивает лучшую визуализацию операционного поля за счет достаточного освещения и оптического увеличения, что в свою очередь позволяет лучше дифференцировать границы тканей, проводить прицельную биопсию, более тщательно осуществлять остановку кровотечения, меньше травмировать окружающую ткань. В то же время лапароскопия является в определенной степени «виртуальной» хирургией, которая практически полностью зависит от правильной работы аппаратуры.
В онкогинекологии в настоящее время лапароскопия может использоваться при раке шейки матки, раке эндометрия, раке яичника и раке вульвы. Однако при каждой из этих локализаций злокачественного процесса лапароскопия имеет строго отведенное ей место.
Так, при всех вышеперечисленных формах рака лапароскопический доступ может применяться для точного хирургического установления стадии заболевания путем ревизии брюшной полости, забрюшинного пространства, широкой лимфодиссекции, биопсии подозрительных участков. При раке эндометрия лапароскопически может быть выполнена и радикальная операция – тотальная лапароскопическая пангистерэктомия в сочетании с тазовой лимфаденэктомией, а при раке шейки матки – лапароскопическая расширенная гистерэктомия тип III по M. Piver (лапароскопический аналог операции Вертгейма) (D. Querleu, E. Leblanc).
Ранее в некоторых клиниках Европы при лечении рака шейки матки в протоколы лечения входила лапароскопическая тазовая лимфаденэктомия с одновременной расширенной влагалищной гистерэктомией по Шаута-Амрейху. Проведение лучевой терапии зависело от состояния удаленных лимфатических узлов.
При раке вульвы лапароскопический доступ используется для выполнения тазовой лимфаденэктомии с целью точного хирургического установления стадии заболевания или же как первый этап радикального хирургического лечения. Особое значение это имеет при уже выявленном поражении илеофеморальных лимфатических узлов.
При раке яичника, помимо уже перечисленных целей, лапароскопия может применяться для выполнения циторедуктивной операции, а также для контроля (возможно, многократного) за эффективностью проводимой адъювантной терапии – second-look лапароскопия, в том числе с использованием специальной канюли для так называемой «динамической лапароскопии».
В случае пограничных опухолей или рака яичника лапароскопия позволяет точно установить стадию заболевания и выбрать соответствующее лечение. Во время лапароскопического вмешательства проводится системная ревизия органов брюшной полости, оценивается состояние лимфатических узлов. В начале операции с особой тщательностью осматривается вся поверхность париетальной и висцеральной брюшины, особенно диафрагма, диафрагмальная поверхность печени, осуществляется забор перитонеальной жидкости или смывов из брюшной полости для последующего цитологического исследования. Из всех подозрительных участков брюшины выполняется биопсия (включая биопсию или соскоб с диафрагмы). Кроме того, при использовании лапароскопического доступа возможно удаление большого сальника на уровне поперечно-ободочной кишки.
Выполненные в США исследования у больных раком яичников (E. Surwit и J. Childers) продемонстрировали огромные возможности лапароскопии в обнаружении микроскопического злокачественного поражения в областях высокого риска: на тазовой брюшине, на большом сальнике, в тазовых и парааортальных лимфатических узлах, в смывах из брюшной полости.
При пограничных опухолях или раке яичника удаление придатков матки или резецированной ткани сохраняемого яичника проводится с соблюдением всех правил абластики с использованием пластиковых эндоскопических контейнеров, в которые помещаются придатки перед их удалением, что предотвращает диссеминацию возможного злокачественного процесса при нарушении целостности капсулы опухоли. Извлечение пластикового контейнера из брюшной полости проводится через троакар 10–12 мм или через заднее кольпотомное отверстие, которое затем зашивается эндоскопическим восьмиобразным швом.
По мнению многих ведущих авторов (D. Querleu, E. Surwit, J. Childers), надежность лапароскопического доступа при выполнении лимфаденэктомии у онкогинекологических больных не уступает таковой при чревосечении при условии выполнения операции опытным хирургом-эндоскопистом, владеющим традиционными хирургическими доступами, при соблюдении основных принципов онкохирургии.
Недавние разработки в технике и методике лапароскопических вмешательств позволили расширить зону выполнения лимфаденэктомии на область общих подвздошных сосудов и, таким образом, в настоящее время имеется возможность проводить полную тазовую лимфаденэктомию. Кроме того, при раке яичника верхней границей лапароскопической парааортальной лимфодиссекции является правая почечная вена. Однако не всем онкогинекологическим больным показана радикальная тазовая лимфаденэктомия, а при начальных стадиях рака шейки матки (IA2 и IB1 стадиях) рекомендуется только подвздошная лимфаденэктомия (D. Dargent).
Следует отметить, что при лимфаденэктомии, выполняемой при раке шейки матки, необходимо удалять запирательные, наружные, внутренние, общие подвздошные группы лимфатических узлов, а при раке эндометрия желательно удалить также парааортальные лимфатические узлы, расположенные ниже нижней брыжеечной артерии. При раке яичника парааортальная лимфаденэктомия должна выполняться от уровня почечных сосудов до малого таза. Необходимость удаления преимущественно той или иной группы лимфатических узлов объясняется особенностями оттока лимфы от органа и особенностями метастазирования опухоли.
Однако во всех случаях рака эндометрия и при начальном раке шейки матки тазовая лимфодиссекция может ограничиваться интерилиакальной областью – зоной, расположенной между наружными и внутренними подвздошными сосудами. Это объясняется тем, что необходимые для удаления лимфоузлы располагаются в этой области, а вовлечение в процесс общих подвздошных и параортальных лимфатических узлов без поражения интерилиакальных встречается довольно редко (менее 2%). Нижней границей лапароскопической лимфодиссекции при раке шейки матки является запирательная ямка.
Молодым женщинам, страдающим раком шейки матки, при выполнении радикальной операции лапароскопическим доступом целесообразно проводить транспозицию обоих яичников наверх в латеральные каналы брюшной полости – удалять их из области последующего лучевого воздействия с целью сохранения их гормонопродуцирующей функции. Причем, на яичники после их транспозиции следует накладывать рентгеноконтрастные скобки для их дальнейшей рентгенологической визуализации.
У молодых нерожавших женщин при микроинвазивном раке шейки матки и даже при наличии выраженной инвазии (стадии IB и IIA) лапароскопический доступ для выполнения тазовой лимфаденэктомии в сочетании с влагалищной радикальной трахелэктомией позволяют сохранять репродуктивную функцию. В литературе описаны более 250 подобных операций, причем в 40% случаев после операции наступила беременность. Следует отметить, что в 3,1% случаев отмечен рецидив заболевания.
В отделении оперативной гинекологии НЦ АГиП РАМН накоплен собственный опыт лечения больных доброкачественными и пограничными опухолями яичника, а также пациенток, страдающих раком шейки и тела матки, в том числе и с использованием лапароскопического доступа. При хирургическом лечении больных раком тела и шейки матки в 24 случаях произведена лапароскопическая лимфаденэктомия. Среди этой группы больных у 17 был плоскоклеточный рак шейки матки IА2-IIВ стадий, а у 7 – аденокарцинома эндометрия.
Техника лапароскопической тазовой лимфаденэктомии заключалась в следующем. Операция выполнялась в условиях пневмоперитонеума 10-15 мм рт. ст. с использованием введенного через пупок лапароскопа и трех троакаров второго прокола, два из которых диаметром 5 мм располагались в подвздошных областях у латеральных краев прямых мышц живота, а один диаметром 12 мм – в надлобковой области по белой линии живота. При выполнении лапароскопической лимфаденэктомии не использовался маточный манипулятор, поскольку большинство подвергающихся этому вмешательству больных страдали раком шейки или тела матки, а сам процесс введения манипулятора мог способствовать диссеминации опухолевого процесса. Париетальная брюшина рассекалась над областью подвздошных сосудов, параллельно ходу наружных подвздошных сосудов, края ее отсепаровывались тупо. Проводилась обязательная визуализация мочеточников. Атравматичными зажимами захватывалась периадвентициальная клетчатка с лимфатическими сосудами и узлами в проксимальной части разреза и тупым путем с помощью закрытого зажима она отслаивалась от фронтальной части наружных подвздошных сосудов, от их медиальных и латеральных стенок, области бифуркации общих подвздошных сосудов. Далее скелетировалась запирательная ямка с тщательным выделением запирательного нерва и, по возможности, единым блоком удалялась клетчатка вместе с лимфатическими узлами, расположенная вокруг внутренних подвздошных сосудов. Отделенная клетчатка с лимфатическими узлами извлекалась под визуальным контролем через 12 мм троакар или помещалась в пластиковый эндоконтейнер с последующей абластичной эвакуацией из брюшной полости. С особой тщательностью выполнялась диссекция лимфатических узлов, расположенных у наружной подвздошной вены. Цепочка лимфатических узлов удалялась, по возможности, единым блоком. Завершающим этапом тазовой лимфаденэктомии было удаление жировой клетчатки с находящимися в ней лимфатическими узлами из пространства между наружной подвздошной артерией и веной. Препараты лимфатических узлов из различных зон таза отправлялись на гистологическое исследование под собственной маркировкой. В ряде случаев перед левосторонней лимфаденэктомией проводилась частичная мобилизация сигмовидной кишки для обеспечения адекватного доступа к области бифуркации общих подвздошных сосудов слева. Для снижения кровопотери при последующей гистерэктомии всегда выполнялась селективная коагуляция маточных артерий у места их отхождения от внутренних подвздошных артерий. В ходе выполнения лапароскопической лимфаденэктомии электрохирургия использовалась только на этом этапе операции.
Лапароскопическая транспозиция яичников была произведена у 3 молодых пациенток, страдающих раком шейки матки. У 1 больной операция завершилась путем чревосечения ввиду больших размеров метастаза в левый наружный подвздошный лимфатический узел и его плотного прикрепления к подвздошным сосудам и стенке таза.
Продолжительность операции составила от 125 до 195 минут, средняя кровопотеря во время вмешательства не превышала 350 мл. В среднем пребывание больной в стационаре после операции составило 7,5 дней.
Следует отметить, что обязательным условием применения лапароскопии у больных раком половых органов является тесное сотрудничество с онкогинекологами, совместный тщательный отбор пациенток для подобных операций, совместное послеоперационное наблюдение и лечение. Так, все онкологические больные, подвергнутые хирургическому лечению в отделении оперативной гинекологии НЦ АГиП, были затем консультированы и при наличии показаний переданы для дальнейшего лечения в ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России.
В июле 2002 г. D. Querleu представил на Международном противораковом конгрессе результаты лапароскопического лечения больных раком, где отметил, что при лапароскопии удаляется столько же лимфатических узлов, сколько и при открытой операции, а 5-летняя выживаемость больных после лапароскопических операций не отличается от таковой у пациенток, прооперированных путем чревосечения.
До настоящего времени роль эндоскопической хирургии при лечении онкогинекологических больных четко не определена, и, по видимому, сейчас среди онкогинекологов имеется больше противников, чем сторонников использования этого доступа. Хотя, без сомнения, интерес к использованию лапароскопии для выполнения лимфодиссекции у онкогинекологических больных значительно возрос, и не только за рубежом, но и у нас в стране появляются публикации о выполнении подобного вмешательства эндоскопическим доступом.
Существует множество вопросов в области применения эндоскопической хирургии в онкологии, на которые еще не даны убедительные ответы. Эта неопределенность подталкивает исследователей различных стран к разработке алгоритмов как предоперационного выбора больных для лапароскопических вмешательств, так и самой методики операции, включая использование новых инструментов и хирургических энергий.
Дискуссионными остаются вопросы о применении лапароскопии при раке яичника, поскольку отсутствуют доказательства надежной абластичности этого вмешательства. В то же время E. Leblanc, D. Querleu и D. Lanvin определяют лапароскопию как «безопасный и точный метод определения стадии заболевания» при раке яичника.
Таким образом, с накоплением хирургического опыта, получением данных о длительности безрецидивного выживания оперированных по представленным методикам больных, разработкой тактики их послеоперационной реабилитации будут даны ответы на дискуссионные вопросы, и это, возможно, позволит изменить всю философию подхода к лечению онкогинекологической патологии и значительно улучшить результаты лечения этой достаточно сложной категории пациенток, снизить затраты на сам процесс лечения и повысить качество жизни страдающих раком женщин
Транспозиция яичников: возможность сохранения репродуктивной функции хирургическим способом

Описать и продемонстрировать новейшую хирургическую методику лапароскопической транспозиции яичников. В данном видео мы представили уникальную малоинвазивную технику транспозиции яичников, в которой доступ к яичникам осуществлен через брюшную полость.
Дизайн: Видео-презентация клинической статьи. В данном видео использованы анимации и демонстрация операции с детальным разъяснением уникальной техники транспозиции яичников. Для данного видео не требовалось одобрение комиссии по биоэтической медицине. В Кливлендской клинике не требуется разрешение данного рода для доклада об одном клиническом случае.
Организация: университет
Пациент: 29-летняя пациентка с диагнозом «рак прямой кишки».
Проведенные манипуляции: Пациенту была выполнена лапароскопическая транспозиция яичников с декортикацией для заморозки овариальной ткани контралатерального яичника. Все манипуляции были выполнены за одну операцию до начала курса химиотерапии и лучевой терапии.
Основные критерии эффективности: Ценность и выполнимость овариальной транспозиции с использованием уникальной техники с возможностью сохранения ретроперитонеального расположения сосудов, кровоснабжающих яичники, с потенциальным сохранением данного кровоснабжения.
Результаты: Создание позадибрюшинного хода (туннеля) с целью его использования для транспозиции яичников — осуществимая и эффективная техника. При проведении лапароскопической транспозиции яичников данная техника может быть применена с целью предотвратить образование крутого разворота в сторону таза сосудов, кровоснабжающих яичники. Все это в совокупности поможет избежать изменений овариального кровоснабжения.
Выводы: Транспозиция яичников является очень хорошей возможностью для сохранения репродуктивной функции хирургическим путем для женщин репродуктивного возраста, кому предстоит краниоспинальное облучение или облучение области малого таза. Эта процедура не представляет клиническую значимость для пациентов, проходящих сопутствующую химиотерапию. Транспозиция яичников может быть выполнена с помощью различных хирургических техник, включая лапаротомические и лапароскопические. В литературе лапаротомическая техника описывается как предпочтительная, поскольку она подразумевает более быстрый период восстановления и менее выраженные послеоперационные боли. Согласно имеющимся публикациям, эффективность данной техники в плане сохранения овариальной функции достигает 88,6% (оценено при помощи измерения уровня гонадотропинов после проведения противоопухолевого лечения).
Транспозиция яичников считается безопасным и эффективным методом хирургической профилактики преждевременного истощения яичников и оптимизации сохранения репродуктивной функции.
Лапароскопическая транспозиция яичников что это
Транспозиция яичников
В настоящее время онкология обладает различными вариантами лечения злокачественных опухолей, которые во многих случаях оказываются эффективны. В связи с этим для ряда больных молодого возраста, перенёсших противоопухолевую терапию, актуальными становятся вопросы качества жизни, сохранения и реализации репродуктивной функции. Особую актуальность эти вопросы приобретают в связи с увеличением случаев рака шейки матки у женщин моложе 30 лет. Врачи не всегда уделяют должное внимание этим аспектам, поскольку пациентки сами сконцентрированы на процессе лечения и редко поднимают эти вопросы (часто просто потому, что они не осведомлены о существующих возможностях лечения).
Как влияет лучевая терапия на функцию яичников?
Негативное влияние на функцию яичников оказывает химиотерапия и лучевая терапия. При облучении области малого таза, паховых и подвздошных областей почти в 100 % случаев возникает аменорея и посткастрационный синдром (преждевременная менопауза, индуцированная лучевой терапией). Влияние лучевой терапии на фолликулярный аппарат яичников является дозозависимым. По данным исследований разрушение 50 % примордиальных фолликулов происходит при облучении в дозе 4 Гр, а доза 5 – 20 Гр достаточна для полного повреждения функции яичников независимо от возраста пациентки. Для возникновения дисфункции матки достаточно дозы 14 – 30 Гр.
Как сохранить функцию яичников при лучевой терапии на область малого таза?
Развития посткастрационного синдрома и повреждения фолликулярного аппарата яичников при лучевой терапии можно избежать путём транспозиции (перемещения) яичников из полости малого таза в брюшную полость. Впервые транспозиция яичников при раке шейки матки была выполнена в 1958 году. Транспозиция яичников за пределы поля облучения и фиксация их в брюшной полости в латеральных каналах по бокам от левого и правого отделов толстой кишки снижает дозу облучения, направленную на яичники. Транспозиция яичников позволяет сохранить нормальный гормональный фон и избежать преждевременной индуцированной менопаузы, а также реализовать репродуктивную функцию в программе суррогатного материнства.
Какие показания для выполнения транспозиции яичников?
Транспозиция яичников показана женщинам репродуктивного возраста перед проведением лучевой терапии на органы малого таза. Показанием для лучевой терапии могут быть онкогинекологические заболевания и другие злокачественные опухоли малого таза. При раке шейки матки IА1 – IIА2 стадий при наличии факторов риска прогрессирования заболевания, как возможных показаний для лучевой терапии, транспозиция яичников может быть выполнена во время выполнения радикальной гистерэктомии. Если же хирургическое лечение пациентке не планируется, то транспозицию яичников выполняют перед лучевой терапией лапароскопическим доступом.
Таким образом, наиболее частые показания для транспозиции яичников является планируемая лучевая терапия по поводу следующих заболеваний:
Какие противопоказания для выполнения транспозиции яичников?
Как выполняетя операция транспозиции яичников?
Операция начинается с пункции брюшной полости специальной иглой и введения в неё нескольких литров углекислого газа. При этом обычно в брюшной полости создаётся давление около 12 – 15 мм рт. ст. Это позволяет приподнять брюшную стенку от внутренних органов и безопасно работать в брюшной полости. Далее в брюшную полость через разрез в области пупка вводят оптическую камеру, которая передаёт изображение на видеомонитор. Через разрезы внизу передней брюшной стенки вводят тонкие рабочие инструменты. Далее выполняю ревизию брюшной полости, оцениваю распространённость онкологического заболевания. При необходимости выполняют биопсию подозрительных участков и берут смывы из брюшной полости для цитологического исследования. После осмотра органов брюшной полости и малого таза окончательно подтверждается спланированный объём операции. Далее левые и правые придатки отсекают от матки и выделяют сосудистые ножки яичников на протяжении 10 – 12 см, образованные яичниковыми артериями и венами. Верхний и нижний полюс каждого яичника помечают металлическими скрепками. Это необходимо для визуализации яичников при рентгенографии брюшной полости для определения из точного местоположения после операции перед проведением лучевой терапии. Далее осуществляют формирование двух забрюшинных туннелей, через которые проводят правый и левый яичники. Яичники фиксируют в конце туннелей по бокам от левого и правого отделов толстой кишки. Яичники с большой вероятностью сохраняют свою функцию, если они были перенесены не менее, чем на 3 см выше верхней границы поля облучения. В конце операции инструменты извлекают, удаляют газ из брюшной полости, на кожные разрезы накладывают внутрикожные косметичные швы.
Какие преимущества имеет лапароскопический доступ?
Лапароскопическая транспозиция яичников является малотравматичной операцией, позволяющей пациентке быстро активизироваться, выписаться из стационара и приступить к основному этапу лечения (лучевой терапии) основного заболевания.
Как контролировать функцию яичников после выполненной транспозиции?
Для оценки состояния и функции яичников можно использовать УЗИ брюшной полости и лабораторные показатели: фолликулостимулирующий гормон (ФСГ), лютеинизирующий гормон (ЛГ), эстрадиол, антимюллеров гормон (АМГ), ингибин В.
Какова эффективность транспозиции яичников?
Около 80 % пациенток, перенёсших лучевую терапию, сохраняют функцию яичников. У 20 % пациенток, тем не менее, происходит снижение функции яичников, видимо, в связи с тем, что пациентки получают небольшую дозу облучения и на поддиафрагмальные пространства. Поэтому для пациенток, которым планируется химиолучевое лечение необходимо предлагать во время транспозиции яичников выполнять дополнительно и криоконсервацию яичниковой ткани.
Размещено в категории: Реконструктивная репродуктивная хирургия